Texto principal:
Aflibercept es un agente anti factor de crecimiento endotelial vascular (FCEV) que ha sido aprobado para el tratamiento de edema macular diabético en Estados Unidos, Unión Europea, Australia y Japón. Existen varios informes sobre la eficacia del tratamiento mediante la medición del espesor de la fóvea central y mejora de la agudeza visual en el ojo contralateral con inyecciones intravítreo de otros agentes anti FCEV como bevacizumab y ranibizumab. El presente creemos es el primer informe sobre mejora de edema macular diabético en el ojo contralateral con inyección intravítreo de aflibercept.
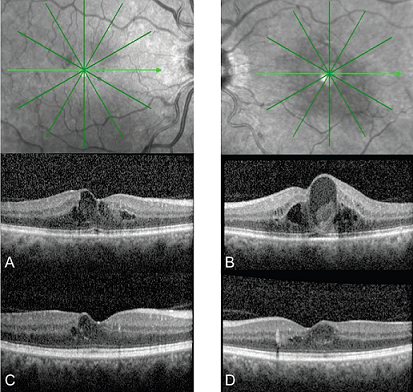
La paciente de 59 años, de raza blanca con antecedentes de diabetes tipo 2 no dependiente de insulina, se presenta para control de retinopatía diabética no proliferativa moderada con edema macular diabético en ambos ojos. La agudeza visual era de 20/40 en ojo derecho y 20/50 en ojo izquierdo. En una consulta anterior, se observó edema leve en ojo derecho. El ojo izquierdo recibió 11 inyecciones de ranibizumab 0,3 mg/0,05 ml en los últimos 13 meses. A pesar de dicho tratamiento la tomografía de coherencia óptica de dominio espectral mostró que el edema había empeorado en ojo derecho y persistía en el izquierdo. (Fig. 1 A y B).
La paciente recibió inyección intravítreo de aflibercept 2 mg/ 0,05 ml en el ojo izquierdo, pero rechazó recibir tratamiento en el otro ojo. A las cuatro semanas, la visión había mejorado a 20/20-1 en ambos ojos y el edema también con un espesor de la fóvea central de 385 y 372 µm en ojo derecho e izquierdo respectivamente (Fig. 1C y D).
Fig. 1. Tomografía de coherencia óptica de ojo derecho (A) e izquierdo (B) con edema macular. Al mes de la inyección intravítreo de aflibercept en ojo izquierdo la OCT muestra mejora del edema macular en ambos ojos (C y D).
A diferencia de bevacizumab y ranibizumab, aflibercept tiene como objetivo el FCEV B y factor de crecimiento placental además del FCEV subtipo A. La vida media de aflibercept en suero es de cinco a seis días, en comparación con dos horas de ranibizumab. Con relación a bevacizumab, aflibercept ha mostrado mayor reducción del nivel en plasma de FCEV, a pesar de tener una concentración inicial menor después de la aplicación. La concentración de FCEV comienza a disminuir a las tres horas de aplicación de aflibercept y bevacizumab.
La reducción de edema macular diabético en el ojo no tratado ha sido informada con bevacizumab y ranibizumab. Dicho efecto es más común con bevacizumab. Existen razones clínicas y farmacoquinéticas que justifican la reducción del edema con bevacizumab en el ojo no tratado. Dada la similitud de la estructura molecular con bevacizumab y el efecto en la concentración de FCEV en suero, aflibercept podría tener los mismos resultados en el ojo no tratado, como se observa en el presente informe. Es necesario realizar nuevas pruebas con aflibercept para seguir estudiando el efecto en el ojo no tratado.
Conclusiones:
La aplicación intravítreo de aflibercept en un solo ojo produce mejora del edema macular diabético en ambos ojos del paciente tratado.
Resumen y comentario objetivo: Dr. Martín Mocorrea