¿Puede la inflamación causar depresión? Me sentí con ánimo descolorido por un día o más después de haber sido vacunado contra la tifoidea. Todos nosotros, probablemente, hemos tenido destellos similares en el estado de ánimo después de una infección o vacunación.
Como anécdota, tales experiencias sugieren que la inflamación podría predecir los síntomas depresivos: el estímulo inflamatorio viene antes de la respuesta depresiva. Pero en el marco dualista cartesiano de la medicina occidental, que separa los polos de la mente y el cuerpo, esta idea de que la inflamación del cuerpo podría predecir la depresión de la mente es perturbadora y exige mucho más que evidencia anecdótica si se debe tomar en serio.
En estudios de seguimiento a largo plazo de muestras de grandes poblaciones, el aumento de las concentraciones en sangre de interleucina 6 o proteína C reactiva predijo la depresión clínica años más tarde. En estudios clínicos de pacientes con hepatitis, evaluados psicológicamente antes y después del tratamiento con interferón, aproximadamente un tercio de los pacientes se deprimieron varias semanas después del tratamiento.
La inflamación de hecho puede preceder a la depresión, en un rango de intervalos de días a décadas. Por lo tanto, es al menos predictivo de la depresión, y por lo tanto podría ser causal, pero ¿cómo?
Es mucho más fácil ahora que hace 30 años, por ejemplo, ver conexiones mecánicas entre el sistema inmune innato y el sistema nervioso central. Resulta que las señales inflamatorias del cuerpo pueden atravesar la barrera hematoencefálica a través de muchos canales de comunicación, incluido el reflejo inflamatorio vagal.
Las ramas extensas del nervio vago pueden detectar una señal inflamatoria en el cuerpo y desencadenar reflexivamente una señal antiinflamatoria del cerebro al cuerpo. Es solo un ejemplo de cómo la supuestamente impregnabilidad similar a un "muro de Berlín" de la barrera hematoencefálica, tradicionalmente concebida en defensa del "privilegio inmunológico" del cerebro, ha sido subvertida desde los años noventa.
Los experimentos con animales muestran que los shocks inflamatorios en el cuerpo, como una inyección de citoquinas, pueden activar la microglía, las células inmunes incrustadas en el cerebro. La activación de las células inmunitarias en el cerebro puede alterar la plasticidad y el desarrollo de las células nerviosas y perturbar el metabolismo neuronal de la serotonina.
La inflamación cerebral hace que los animales se comporten como si estuvieran deprimidos, se retiran socialmente y pierden su preferencia normal por el agua endulzada y otras recompensas. En general, hay evidencia de estudios en animales para una cadena explicativa de flechas causales desde el sistema inmunitario periférico, el sistema nervioso central y conductas cuasi depresivas.
Si esta cadena causal demuestra ser igualmente válida en los humanos, entonces es mecánicamente plausible que los medicamentos antiinflamatorios puedan tener efectos antidepresivos. La evidencia hasta la fecha no es más que un apoyo parcial de esta propuesta terapéutica y mucho depende de lo que entendemos por depresión.
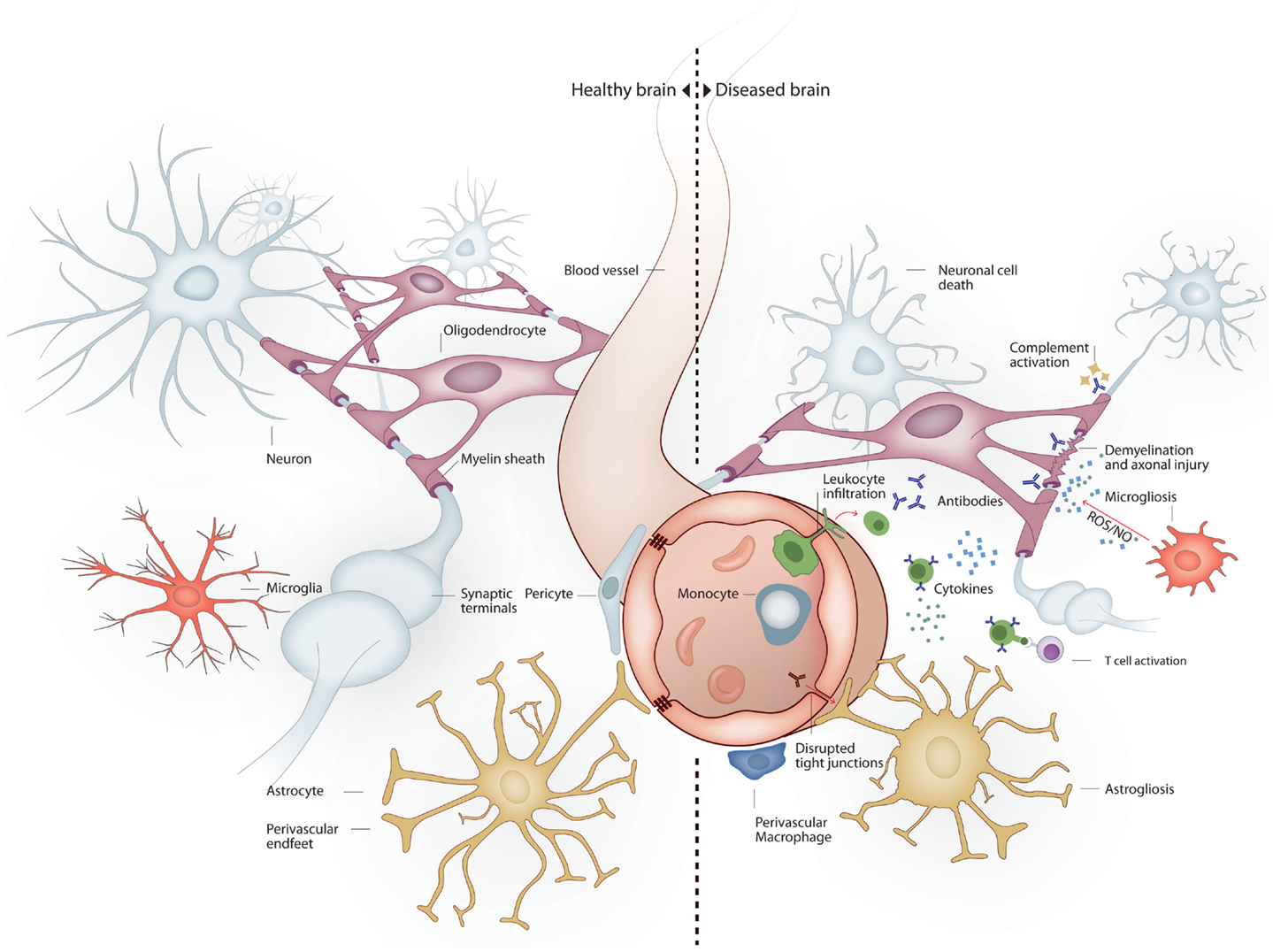
Cambios en el medio cerebral en respuesta a la inflamación sistémica.
Hasta ahora, he usado la palabra ampliamente para abarcar una gama de experiencias desde un cambio de humor posterior a la vacunación hasta un episodio más grave de depresión clínica. Esto es compatible con los datos epidemiológicos que muestran que los síntomas depresivos son comunes y se distribuyen continuamente entre nosotros; todos estamos en algún lugar en un espectro de humor.
Sin embargo, la depresión en la formulación del trastorno depresivo mayor (TDM) es un diagnóstico categórico: TDM, ¿sí o no? Esta decisión binaria se basa en los síntomas clínicos, como mal humor, pérdida de placer y fatiga.
No se necesitan análisis de sangre, escáneres cerebrales ni biomarcadores para hacer un diagnóstico de TDM. Y los pacientes que tienen análisis de sangre o escaneos cerebrales anormales como resultado de un trastorno inflamatorio no son técnicamente elegibles para un diagnóstico de TDM. En cambio, pueden ser diagnosticados como casos de la llamada depresión comórbida.
Los síntomas de la depresión comórbida se han medido como puntos finales secundarios en ensayos clínicos aleatorios diseñados para probar el efecto de un fármaco antiinflamatorio en un punto final primario relacionado con los síntomas de salud física de un trastorno inflamatorio.
Las puntuaciones de depresión comórbida se han combinado de forma metaanalítica y hay evidencia de un efecto antidepresivo de los fármacos antiinflamatorios. Pero ha sido difícil descartar la posibilidad de que los pacientes con depresión comórbida tengan una mejor salud mental después del tratamiento antiinflamatorio como consecuencia indirecta, un epifenómeno psicológico, del efecto primario del fármaco en su salud física.
Para estar seguros de que los medicamentos antiinflamatorios pueden tener efectos antidepresivos, se deben realizar más ensayos clínicos en pacientes deprimidos sin trastornos inflamatorios importantes. Se han informado menos de diez ensayos de AINE para el TDM, en su mayoría ensayos pequeños con menos de 50 participantes por estudio. Combinando estos datos de forma metaanalítica, no hubo un efecto de tratamiento significativo en el cambio controlado con placebo de las puntuaciones iniciales en una escala de síntomas depresivos.
En el único ensayo publicado de un anticuerpo anticitoquina para el TDM, los pacientes con biomarcadores evidencian niveles más altos de inflamación periférica antes del tratamiento tuvieron un mayor beneficio antidepresivo del tratamiento con anticuerpos anti-TNF.
Un pesimista razonable podría concluir que el vaso está más vacío que lleno y que la inmunoterapia tiene un futuro incierto en psiquiatría. Alternativamente, el poder estadístico de estos ensayos podría haber sido comprometido por el reclutamiento de pacientes con TDM independientemente de su estado de inflamación; aunque sabemos que no todos los pacientes deprimidos están inflamados y no hay ninguna razón para esperar que cualquier medicamento antiinflamatorio funcione como una panacea para la depresión, beneficiando milagrosamente incluso a aquellos pacientes que no están inflamados.
Un mayor uso de biomarcadores será clave para desbloquear el potencial terapéutico de la inmunopsiquiatría. Existe una gran cantidad de métodos disponibles para medir el estado periférico del sistema inmunitario innato, incluida la citometría, la expresión génica y los ensayos funcionales.
Aún no sabemos cuál de los muchos biomarcadores potencialmente medibles a partir de una muestra de sangre podría ser más sensible y confiable para predecir la probabilidad de respuesta de un paciente deprimido a una intervención antiinflamatoria.
Si se pueden validar estos biomarcadores, eso podría ayudarnos a pasar de la estancamiento terapéutico actual y un nivel de inversión desproporcionadamente bajo en el desarrollo de fármacos antidepresivos. De manera más amplia, y especulativa, las implicaciones terapéuticas de la depresión inflamada podrían incluso ir más allá de las drogas.
La estimulación vagal funciona para algunas personas con depresión
La estimulación del nervio vago (VNS) ha sido autorizada como tratamiento para la depresión en los EE. UU. desde 2005, pero su eficacia clínica y su mecanismo de acción siguen siendo controvertidos. Ahora sabemos que estimular el nervio vago amplifica su señal antiinflamatoria. Esto podría explicar por qué la estimulación vagal funciona para algunas personas con depresión.
En el futuro, tal vez, podríamos predecir los efectos antidepresivos de la estimulación vagal por los biomarcadores inmunes para que los costos y riesgos de implantar quirúrgicamente un dispositivo de estimulación no sean incurridos por pacientes que probablemente no se beneficiarán. Y se han recomendado enfoques alternativos a la estimulación vagal, desde estimuladores externos hasta yoga, meditación y ejercicio físico. Estas intervenciones seguras y accesibles podrían evaluarse aún más para determinar la eficacia antiinflamatoria y antidepresiva.
El sistema inmunitario innato se activa cuando los animales o los seres humanos están estresados o amenazados socialmente
El estrés social y psicológico es el principal factor de riesgo conocido para la depresión, pero no ha sido tan claro cómo el estrés causa la depresión de manera mecánica. Ahora sabemos que el sistema inmunitario innato se activa cuando los animales o los seres humanos están estresados o amenazados socialmente. Y hace tiempo que sabemos que el sistema inmunológico tiene una memoria de amenazas biológicas (p. Ej., infecciones) que se encuentran en la infancia.
Si supiéramos más acerca de la memoria del sistema inmunitario para las amenazas sociales en la infancia (por ejemplo, la separación de un padre), ¿nos ayudaría a intervenir de manera más efectiva para prevenir y mitigar los impactos de la adversidad de la vida temprana en la salud mental de los adultos?
Aunque el caso de la depresión inflamada parece cada vez más interesante, aún existen muchos riesgos sobresalientes. La principal advertencia clínica es la ausencia de datos positivos de un ensayo antidepresivo diseñado prospectivamente de una intervención antiinflamatoria.
También es problemático que no tengamos buenos biomarcadores para la inflamación del cerebro humano: las únicas opciones son el muestreo del líquido cefalorraquídeo, que puede causar un fuerte dolor de cabeza o una tomografía por emisión de positrones, que está limitada por la falta de radiotrazadores específicos y sensibles para microglial activación. Y los riesgos de seguridad de los medicamentos antiinflamatorios, como la reducción de la resistencia a las infecciones, aún no se han sopesado en comparación con sus posibles beneficios antidepresivos.
Un riesgo científico clave es la ausencia de evidencia genética para los mecanismos inflamatorios de la depresión, que refleja los desafíos de larga data en la determinación de los riesgos genéticos para el trastornos depresivo mayor per se.
Los estudios de asociación de todo el genoma solo se han vuelto lo suficientemente grandes como para identificar de manera robusta un conjunto de genes enriquecidos para funciones neuronales y algunas funciones inmunitarias que representan menos del 10% del riesgo del trastornos depresivo mayor.
Aún debemos aclarar el impacto inflamatorio de estos y otros genes de riesgo que podrían surgir en el futuro, teniendo en cuenta que las interacciones entre el gen y el ambiente probablemente sean importantes para explicar las diferencias individuales en la respuesta depresiva o la resistencia a las tensiones ambientales.
Y las marcas epigenéticas pueden llevar una memoria inmunológica del estrés social desde la infancia hasta la vida posterior, como lo sugieren los experimentos con animales. Pero todo esto queda por ser probado científicamente y resuelto en humanos.
La configuración dualista de los servicios especializados probablemente perjudica a muchas personas que viven con síntomas físicos y mentales
A fin de cuentas, creo, las oportunidades superan los riesgos. Incluso podría haber posibilidades de impacto terapéutico, no solo a lo largo de las décadas necesarias para el desarrollo de fármacos, sino también de manera más inmediata.
A partir de ahora, la mayoría de los servicios de atención secundaria de la salud están especializados en medicina para el tratamiento de la inflamación o en psiquiatría y psicología para tratar la depresión. Esta configuración dualista de los servicios especializados probablemente perjudica a muchas personas que viven con síntomas físicos y mentales.
El fortalecimiento de la evidencia científica de que la depresión y la inflamación están causalmente vinculadas entre sí y que el entorno social podría hacer que los servicios de atención de salud física y mental se unan más en el momento de la asistencia para que cada paciente sea tratado como una unidad (persona) y por un equipo.

Edward Bullmore. Trabajo medio tiempo en la Universidad de Cambridge como profesor y jefe del Departamento de Psiquiatría y medio tiempo en GlaxoSmithKline R&D como director principal de inmuno-psiquiatría y soy un psiquiatra consultor honorario y director de investigación y desarrollo en Cambridgeshire y Peterborough NHS Fundación Trust.