|
Resumen
|
| Introducción |
La piodermia gangrenosa (PG) es una dermatosis inflamatoria reactiva no infecciosa que se halla dentro del espectro de las dermatosis neutrófilas.
Este grupo de dermatopatías incluye al síndrome de Sweet y al síndrome de Behcet. La incidencia es de aproximadamente 0,63 por 100000 y la media de edad al comienzo es de 59 años. La incidencia según el sexo oscila desde ser igual en ambos sexos a que las mujeres sean las más afectadas en hasta el 76% de los casos.
| Cuadro clínico |
La PG clásica suele ser una lesión eritematosa sumamente dolorosa que progresa rápidamente a una úlcera ampollosa o necrótica. Con frecuencia tiene un borde violáceo/eritematoso irregular. La más afectada es la pantorrilla, aunque la PG puede aparecer en cualquier parte del cuerpo. La lesión se puede desencadenar por un traumatismo leve, fenómeno conocido como ‘patergia’.
| Las lesiones de la PG demasiado frecuentemente se diagnostican como úlceras que no cicatrizan y los pacientes son sometidos a desbridamiento, que puede producir un deterioro catastrófico a través de esta respuesta patérgica. |
La enfermedad afecta predominantemente a adultos, pero hay algunos raros casos infantiles. La mayoría de los pacientes no tienen antecedentes familiares de la enfermedad.
Aproximadamente el 85% de los casos de PG son del tipo ulceroso, si bien hay otros subtipos: ampolloso, vegetativo, pustuloso, periostomal y variantes granulomatosas superficiales. Los diferentes subtipos a veces cambian de uno a otro.
El diagnóstico diferencial debe incluir todas las demás causas de úlceras cutáneas, ya que no hay criterios de laboratorio o histopatológicos definitivos.
La PG también puede afectar sitios extracutáneos como los ojos (escleritis, úlcera córnea,) los pulmones (nódulos pulmonares asépticos) y el bazo.
> PG clásica
La forma más frecuente de PG es una úlcera dolorosa rápidamente progresiva con un borde irregular violáceo (Fig 1).
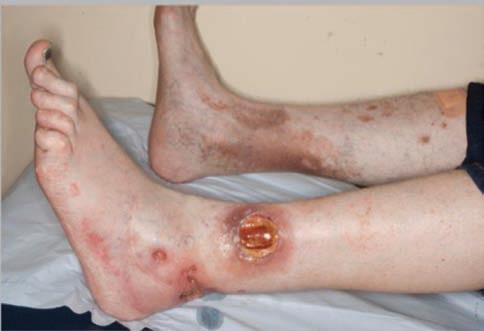
Figura 1
> PG ampollosa
Esta forma se manifiesta con vesículas y ampollas superficiales dolorosas de evolución rápida y que surgen en olas; a menudo se unen entre sí, sobre todo en los brazos. Histológicamente es similar al síndrome de Sweet. Se debe investigar la presencia de una neoplasia maligna hematológica, ya que éstas se identifican en hasta el 70% de los casos.
> PG pustulosa
Esta forma se ve con mayor frecuencia en la reagudización de la enfermedad intestinal inflamatoria y se manifiesta con pústulas dolorosas sobre una base eritematosa, a menudo en las superficies extensoras.
> PG granulomatosa superficial PG
Conocida como PG vegetativa, este subtipo habitualmente progresa con mayor lentitud y tiene lesiones verrugosas y ulcerosas.
> PG Periostomal
Esta variante probablemente se produce por una respuesta patérgica al trauma por irritación fecal o secundaria a aparatos en la piel y se la ve con frecuencia en pacientes con ostomías debido a enfermedad intestinal inflamatoria.
> Piodermia maligna
Es una variante clínica importante, pero rara, en la que se observa una ulceración destructiva que afecta la parte superior del torso, la cabeza y el cuello. Las lesiones no muestran el borde violáceo que se observa en la PG clásica y no se asocia con enfermedad sistémica.
| Etiología |
Se encuentran enfermedades sistémicas de base en hasta el 50% de los casos, de modo que es necesario identificarlas tras efectuar el diagnóstico de PG.
Las más frecuentes son la enfermedad intestinal inflamatoria en hasta el 30% de los casos, las artritis reumatoide y las artrítides seronegativas en hasta el 10%, neoplasias hematológicas malignas, gammapatías monoclonales (en especial la gammapatía tipo inmunoglobulina A) en el 5% y otras neoplasias en el 5% de los casos.
Se ha implicado a fármacos como propiltiouracilo, inhibidores de la tirosina-cinasa, inhibidores del TNFα y del factor estimulante de colonias de granulocitos pero el factor desencadenante puede ser la enfermedad para la que se recetaron estos medicamentos.
También hay síndromes asociados con la PG, entre ellos PG con acné quístico e hidradenitis supurativa, (PASH), PG con artritis piógena y acné (PAPA), y PG con artritis piógena, acné e hidradenitis supurativa.(PAPASH)
| Fisiopatología |
La patogénesis de la PG aún no se conoce bien, si bien se reconoce que los neutrófilos tienen un papel fundamental. Se identificó el aumento de varios factores clave proinflamatorios y quimiotácticos de los neutrófilos dentro de la piel de las lesiones, entre ellos IL-1β, IL-17, TNFα, IL-8, IL-6, IL-17 and IL-23.
También aumenta la expresión de la metaloproteinasa de la matriz, en especial la MMP 9 y 10, que podrían contribuir a la mala cicatrización junto con la expansión clonal de las células T que se identificó en la piel o el plasma de pacientes con PG. El papel exacto de los linfocitos en la patogénesis de la PG aún se debe dilucidar.
Hasta ahora se comprobó una base genética para la PG en los cuadros sindrómicos con mutaciones en el gen PSTP1P1 / CD2BP1 en los síndromes PAPA y PASH. Normalmente la pirina inhibe la activación del inflamasoma, pero el mutante PSTPIP1 inhibe el efecto anti-inflamatorio de la pirina y esto produce la liberación de citosinas proinflamatorias.
| Datos Histológicos |
La PG sigue siendo un diagnóstico clínico y a veces difícil. La biopsia de piel es útil para descartar otras causas de ulceración cutánea y para enviar las muestras para cultivos bacterianos, micobacterianos y micóticos.
Debe incluir el borde activo de la úlcera y penetrar hasta los tejidos subcutáneos. Se debe advertir a los pacientes que este procedimiento siempre causa el agrandamiento de la úlcera, así como que también puede inducir una respuesta inmunológica patérgica al trauma.
Los resultados histológicos dependen del lugar de la biopsia y la edad de la lesión. En la PG ulcerosa clásica puede haber ulceración de la epidermis y la dermis asociada con un intenso infiltrado neutrófílo, pústulas neutróflilas y formación de abscesos.
Se podrán observar distintos datos histológicos según la variante clínica. A veces se identifica histológicamente vasculitis, que puede ser secundaria a la úlcera. Si se identifica una vasculitis verdadera se deben investigar sus causas.
| Diagnóstico |
Hasta ahora no hay criterios clínicos o anatomopatológicos validados para diagnosticar PG. Maverakis et al propusieron nuevos criterios basados sobre un consenso internacional de especialistas, que exige un criterio principal y cuatro criterios secundarios.
Cuadro 1 Herramienta diagnóstica mejorada para la piodermia
|
Criterios principales
Criterios secundarios
|
(Véase Cuadro 1). Si bien aún no se ha adoptado ampliamente, con este método la PG ya no es un diagnóstico de exclusión.
| Diagnóstico diferencial |
Se deben tener en cuenta otras causas de úlceras cutáneas. Entre ellas es necesario considerar enfermedades arteriales y venosas, causas hematológicas (drepanocitosis, crioglobulinemia y síndrome antifosfolipídico), oclusión vascular, vasculitis, infecciones, calcifilaxia, úlceras inducidas por fármacos, tumores primarios o metastásicos, hipertensión (úlcera de Martorell) y otras enfermedades inflamatorias como la enfermedad de Crohn cutánea.
> Cómo abordar al paciente
Una anamnesis exhaustiva es clave, con la averiguación específica sobre una posible respuesta patérgica a traumas leves o importantes, así como antecedentes de dolor, progresión rápida, síntomas que sugieren infección o enfermedad sistémica y antecedentes detallados sobre la historia de ingesta de fármacos.
El examen clínico de la úlcera y el examen de todo el cuerpo son esenciales, así como la biopsia de piel.
Los estudios complementarios deben incluir:
- Hemograma completo
- Eritrosedimentación
- Proteína C-reactiva
- Pruebas funcionales hepáticas y renales
- Electroforesis de proteínas
- Proteína urinaria de Bence Jones
- Pesquisa completa de hepatitis
- Pesquisa vasculítica
- Crioglobulinas si los antecedentes son sugestivos
- Pruebas de coagulación para investigar causas trombóticas de úlceras.
Se aconseja la calprotectina fecal ante la sospecha clínica de enfermedad intestinal inflamatoria.
También están indicadas la radiografía de tórax antes del tratamiento sistémico y la tomografía computarizada (TC) si se sospecha una neoplasia subyacente.
| Tratamiento |
Solo hay dos estudios aleatorizados controlados sobre el tratamiento de la PG y tampoco existen guías nacionales o internacionales. El tratamiento por lo tanto es problemático y se basa sobre la gravedad de la PG (Figura 2).
El tratamiento de primera línea, que optimiza el cuidado local de la lesión, es especialmente importante en los casos de PG en la pierna, donde la cicatrización de la herida puede demorar debido a enfermedad vascular.
El tratamiento de apoyo, con vendajes o apósitos apropiados, la compresión (si se descartó la insuficiencia arterial) y la analgesia adecuada son esenciales para optimizar la cicatrización.
Los corticoides tópicos potentes y el ungüento de tacrolimus aplicado a la superficie de la úlcera son útiles y se pueden considerar las inyecciones de conticoides en el borde activo eritematoso.
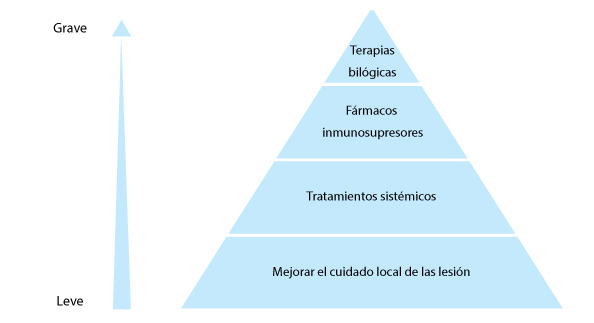
Figura 2. Selección del tratamiento basado sobre la gravedad y extensión de la piodermia gangrenosa.
Adaptado de George C, et al.
La enfermedad más grave exige tratamiento sistémico.
Los corticoides por vía oral (0,5–1 mg/kg/día) son el pilar del tratamiento y tienen efectos rápidos.
La ciclosporina se puede emplear sola o asociada con corticoides como agente ahorrador de estos, en casos donde el tratamiento prolongado es necesario. En un estudio multicéntrico aleatorizado controlado de 121 pacientes, se comparó entre prednisolona 0,75 mg/kg/día (dosis máxima 75 mg) y ciclosporina 4 mg/kg/día (dosis máxima 400 mg). Se logró la remisión a 6 meses en solo el 50% de los pacientes y no hubo diferencia significativa entre los tratamientos.
La metilprednisolona intravenosa por pulsos puede ser útil para iniciar una respuesta rápida si se la da junto con inmunospresores como metotrexato, micofenolato mofetil, ciclofosfamida, azatioprina e inmunogloblina intravenosa en altas dosis.
Un conjunto importante de datos apoya el tratamiento biológico para la PG dirigido contra varias citocinas, pero no hay consenso sobre si estos tratamientos se deben administrar solo ante el fracaso de otros o como tratamiento de primera línea en la PG grave
Hasta ahora infliximab es el agente con la mayor evidencia para apoyar su empleo temprano en la PG. En un estudio aleatorizado controlado sobre infliximab (5 mg/kg intravenoso) versus placebo, el 69% de los pacientes tuvo mejoría clínica en la semana seis tras una sola infusión.
Un estudio de observación retrospectivo mostró la curación más rápida de las lesiones en una proporción significativa de pacientes tratados con infliximab y adalimumab versus los corticosteroides orales solo. Esto apoya aún más la idea de que el tratamiento biológico se debe considerar como una estrategia terapéutica temprana.
Adalimumab mostró ser eficaz para lograr la cicatrización de la lesión en casos recalcitrantes y hay casos clínicos que demuestran buenos resultados con etanercept, ustekinumab, anakinra y canakinumab.
| Comentario |
A pesar de ser un problema bien conocido, la PG no se suele diagnosticar tempranamente.
Es importante que todos los médicos estén bien informados sobre este trastorno y tengan en cuenta la PG cuando evalúan pacientes con úlceras, ya que el tratamiento apropiado rápido en una etapa temprana der la enfermedad puede evitar las complicaciones del tratamiento sistémico prolongado, el retraso en la cicatrización de las lesiones y las cicatrices.
Resumen y comentario objetivo: Dr. Ricardo Ferreira