En los pacientes graves, la natremia puede estar alterada por muchos factores. El 60% a 70% del cuerpo humano está compuesto por agua, y aproximadamente el 30% de esa agua corresponde al líquido extra celular, siendo el cloruro de sodio (ClNa) el principal electrolito (135-145 mEq/L). la hiponatremia ocurre cuando el sodio sérico es <135 mEq/L; es la anormalidad electrolítica más común en los pacientes hospitalizados, y se presenta en el 30% de los pacientes internados en la unidad de terapia intensiva (UTI). Un nivel de sodio sérico <125 mEq/L es un predictor independiente de mortalidad, en especial en los enfermos críticos, y debe ser corregida o evitada.
El síndrome de secreción inadecuada de hormona antidiurética (del inglés: SIAHD) y de depleción cerebral de sal (wasting syndrom) (del inglés: CSW) representan un subgrupo particularmente problemático de hiponatremias. Estas condiciones son muy comunes en los paciente con trastornos intracraneanos y afecciones neuroquirúrgicas pero también pueden observarse en otra poblaciones de enfermedades críticas. En la población neuroquirúrgica, el 62% de las hiponatremias está ocasionado por el SIADH, y el 4,8% a 31,5%, por el CSW. Estas 2 condiciones son muy similares y en los pacientes críticamente enfermos pueden ser de difícil diferenciación.
Fisiopatología
La hiponatremia puede asociarse con osmolalidad elevada, baja o normal. La osmolalidad normal es de 280 y 295 mOsm/L y puede medirse en el suero o calcularse mediante la fórmula siguiente:
[2 × Na] + [N ureico en sangre/2,8] + [glucosa/18].
La determinación de la osmolalidad es el primer paso en la evaluación de las hiponatremias.
Osmolalidad normal y elevada
En general, la hiponatremia con osmolalidad normal relacionada con la seudohiponatremia o hiponatremia “falsa”. Su etiología incluye a la hiperlipidemia, la hiperproteinemia y los errores de laboratorio. La hiponatremia con osmolalidad elevada indica un exceso de solutos más que de sodio, incluyendo la glucosa, el manitol y el propilenglicol (un excipiente de algunos medicamentos intravenosos). El exceso de osmolalidad por hiperglucemia u otras sustancias hace que el agua del espacio intracelular pase al compartimiento extracelular, disminuyendo de ese modo los valores del sodio sérico.
Osmolalidad baja, SIADH y CSW
La hiponatremia con osmolalidad baja o hipotonicidad se divide en 3 categorías, dependiendo de la volemia del paciente:
1) Hipervolemia con osmolalidad baja: causada por el excedente de agua. Generalmente, la insuficiencia cardíaca, la cirrosis hepática y el síndrome nefrótico se suelen asociar con retención de agua, provocando hipervolemia e hiponatremia por dilución.
2) Hipotonicidad con hipovolemia: comúnmente provoca la pérdida excesiva de agua. Las causas incluyen los vómitos, la diarrea, la pérdida excesiva de agua/sudoración, la hemorragia, el uso de diuréticos y la insuficiencia suprarrenal. El CSW es una forma de hipoosmolalidad hipovolémica, la cual a menudo está relacionada con un trastorno del sistema nervioso central o neuroquirúrgico. El mecanismo exacto de este síndrome se desconoce, pero el resultado final es el aumento de la excreción de agua con disminución de la natremia y aumento del sodio urinario.
3) Hipotonicidad euvolémica: está ocasionada por la ingesta excesiva de agua (en general psicógena), la insuficiencia renal, la insuficiencia suprarrenal, el hipotiroidismo y, con mayor frecuencia, el SIADH. La osmolalidad sérica está regulada principalmente por la hormona antidiurética (ADH) o arginina vasopresina y los riñones. Ante un aumento de la osmolalidad, la hipófisis libera ADH para reducir el volumen intravascular, aunque el desencadenante principal es la hiperosmolalidad. La ADH se une a los receptores de vasopresina en los riñones, provocando la reabsorción de agua sin reabsorción de sodio. La liberación de ADH en presencia de una osmolalidad sérica normal o baja es considerada “inadecuada”, ya que el agua continúa siendo reabsorbida por lo riñones, disminuyendo el nivel sérico de sodio y aumentando el nivel del sodio urinario. Los riñones todavía son capaces de excretar sodio normalmente, porque su excreción está regulada por la aldosterona y el péptido natriurético auricular. Este proceso da como resultado una orina concentrada, con un nivel elevado de sodio y aumento de la osmolalidad. En el SIADH, la osmolalidad urinaria permanece constante porque los cambios en la ingesta de agua/osmolalidad no afectan la secreción de ADH, y por lo tanto, la cantidad de agua excretada en la orina no se modifica. Las causas del SIADH son los trastornos del sistema nervioso central, los trastornos pulmonares, las neoplasias, la cirugía y ciertos medicamentos.
.png)
Síntomas
Los síntomas de hiponatremia comúnmente dependen de la agudeza y la gravedad del descenso del sodio. Una disminución más lenta o leve de la natremia puede asociarse ir acompañada de anorexia, cefalea, irritabilidad y debilidad muscular. Un subgrupo importante de pacientes es asintomático. Los síntomas más graves que siguen al descenso rápido del sodio o a una natremia <120 mEq/L son: edema cerebral, náuseas, vómitos, delirio, alucinaciones, letargo, convulsiones, paro respiratorio y, potencialmente, muerte. La volemia también influye en otros síntomas que experimenta el paciente. La evaluación de la volemia es importante para ayudar a determinar la causa de la hiponatremia y cuál es el tratamiento óptimo.
Diagnóstico
La diferenciación entre el SIADH y el CSW puede ser difícil pero es muy importante para determinar la estrategia terapéutica apropiada. Ambas condiciones se encuentran en pacientes internados en UTI. En los dos síndromes, los pacientes presentan hiponatremia hipotónica, con osmolalidad <280 mOsm/L, natremia <135 mEq/L y sodio urinario elevado, por lo general >50 mEq/L (normal 20-40 mEq/L). La diferencia principal entre el SIADH y el CSW es la volemia. Los pacientes con SIADH son euvolémicos o levemente hipervolémicos, mientras que los pacientes con CSW son hipovolémicos. Los signos de depleción de volumen, como la hipotensión ortostática, la disminución de la presión venosa o de la presión capilar pulmonar en cuña, el aumento del hematocrito y los signos físicos de deshidratación hacen sospechar la presencia de CSW y no de SIADH.
Velocidad de la corrección
La hiponatremia debe corregirse lentamente durante el tratamiento, a una velocidad de 8-12 mEq/L en 24 horas o 0,5 mEq/L/hora. La corrección rápida del nivel de sodio en la hiponatremia se ha asociado con mielinólisis pontina central, un trastorno irreversible que afecta a la sustancia blanca pontina y causa trastornos mentales, cuadriplejía fláccida, anormalidades de los nervios craneanos, pasaje del agua desde el espacio intracelular hacia el extracelular, falso descenso de la natremia y coma. Los pacientes que desarrollan hiponatremia más rápidamente tienen mayor morbilidad y mortalidad causadas por esa condición. Los pacientes con hiponatremia aguda pueden tolerar una corrección más rápida de su natremia que los que sufren hiponatremia crónica, sin tanto riesgo de mielinólisis pontina central. Durante la corrección habrá que monitorear frecuentemente la natremia (por ej., c/6-12 horas), cuyo nivel objetivo durante el tratamiento de la hiponatremia es 130-135 mEq/L, siendo 135 mEq/L el límite inferior normal. A menudo, esta estrategia permite revertir los síntomas y evitar el exceso de corrección de los niveles de sodio.
Opciones terapéuticas
El primer paso en el tratamiento del SIADH o el CSW es la identificación de la causa para luego revertirla o tratarla. Las causas reversibles más comunes de SIADH son los medicamentos, como la carbamazepina, la oxicarbazina, la ciclofosfamida y los inhibidores selectivos de la recaptación de serotonina, y la enfermedad pulmonar como la neumonía. El SIADH inducido por medicamentos puede revertir suspendiendo la medicación y el SIADH causado por una neumonía puede revertir mediante el tratamiento de la neumonía. Lamentablemente, muchas causas comunes del SIADH y el CSW, como la hemorragia subaracnoidea y las neoplasias, son irreversibles, al menos en el corto plazo. El próximo paso es iniciar el tratamiento de la hiponatremia.
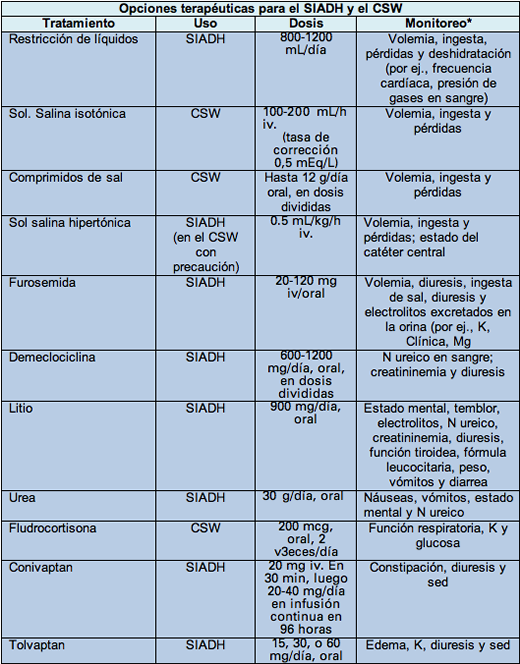
*Además de monitoreo de la natremia
El uso de todos los agentes revisados para el tratamiento del IADH y el CSW se considera no autorizado, con excepción de los antagonistas de la vasopresina.
Restricción de líquidos
La restricción de líquidos es una opción para los pacientes con SIADH pero no para los pacientes con CSW, porque ya tienen hipovolemia, lo que subraya aún más la importancia de diferenciar ambas condiciones. La restricción de líquidos es especialmente peligrosa en los pacientes con hemorragia subaracnoidea, porque la depleción de volumen podría aumentar el riesgo de vasoespasmo. En el SIADH, la cantidad total de ingesta líquida debe ser inferior a las pérdidas totales (orina y pérdidas insensibles). La restricción de líquidos entre 800 y 1.200 mL/día es efectiva tanto en el SIADH agudo como en el crónico. Sin embargo, en los pacientes con SIADH la sed es normal, de manera que la restricción de líquido puede crear disconfort y dificultar su cumplimiento. La restricción de líquido puede ser difícil de mantener en la UTI debido a las infusiones continuas, la administración de antibióticos intravenosos y de otros medicamentos que obligan al paciente a ingerir líquidos.
Solución salina isotónica
El tratamiento principal del CSW es la reposición de líquido con ClNa isotónico (0,9%), o solución salina normal. El primer paso en el tratamiento del CSW es reponer el volumen intravascular y mantener neutro el equilibrio líquido. El requerimiento total del líquido necesario para reponer el volumen puede calcularse comenzando con el déficit de sodio, el cual se determina restando el sodio del paciente de un nivel de sodio normal (por ej., 140 mEq/L) y dividiéndolo luego por 2 (por ej., [{140} – Na / 2]). El próximo paso es calcular el déficit de sodio corporal total según la talla del paciente, usando la fórmula siguiente: (déficit de Na × [0,6 × kg de peso corporal]). La velocidad de reposición del sodio debe ser de aproximadamente 0,5 mEq/hora para evitar la corrección rápida; el déficit de sodio (en mEq) / 0,5 (objetivo de la velocidad de reposición de sodio en mEq/h) es igual a la cantidad de horas en las que se debe reponer el sodio. Por último, la velocidad de la infusión del ClNa (en mL/hora) se determina usando la fórmula siguiente: [déficit corporal total de Na / 0,154 mEq/mL] / total de horas).
|
Ejemplo de cálculo para el aporte de ClNa en el CSW Datos del paciente para el cálculo Natremia = 124 mEq /L Déficit de Na (140 -124 mEq /L) / 2 = 8 mEq /L Déficit de Na corporal total 8 mEq/L × (0,6 L /kg × 68 kg) = 326,4 mEq Horas totales para la corrección 8 mEq /L ÷ 0,5 mEq /h = 16 horas Velocidad de infusión del ClNa (326,4 mEq / 0,154 mEq /ml) / 16 h = 132,5 ml / hora |
Una vez que el paciente es rehidratado, el mantenimiento del estado euvolémico se puede considerando la entrada de líquidos y la diuresis. Aunque el tratamiento de primera línea para el CSW es el ClNa, no suele corregir por completo la natremia.
Comprimidos de sal
Para reponer la pérdida de sodio por los riñones que ocurre en el CSW se pueden usar comprimidos orales de sal. El objetivo terapéutico es crear un balance positivo de sodio. En este síndrome se han utilizado hasta 12 g/día de ClNa en comprimidos, en dosis divididas. El agregado de comprimidos de sal se suele hacer cuando la natremia sigue baja a pesar de la reposición adecuada del volumen.
Solución salina hipertónica
En el SIADH, la excreción renal de sodio permanece intacta, de manera que el sodio administrado mediante líquidos intravenosos se excretará en la orina. Este concepto es diferente del que guía la reposición de líquidos en la hipovolemia, en la cual tanto el sodio como el agua son retenidos en el espacio intravascular. Por esta razón, para el tratamiento del SIADH, en vez del ClNa se prefiere la solución salina hipertónica. La osmolalidad del ClNa al 3%, que es la concentración de solución salina hipertónica más comúnmente usada, es 1.027 mOsm/L, mientras que la osmolalidad del ClNa es 308 mOsm/L. Cuando se administra a los pacientes con SIADH, puede empeorar la hiponatremia debido a que la osmolalidad del ClNa es inferior a la osmolalidad de la orina del paciente.
La solución salina hipertónica ≥3% debe administrase a través de un catéter venoso central. La infusión continua de sodio al 3% se debe hacer a una velocidad de 0,5 mL/kg/hora, para aumentar el sodio sérico a razón aproximadamente de 0,5 mEq/L/hora. Se debe monitorear la natremia con sumo cuidado durante el tratamiento con solución salina hipertónica, ya que a veces la velocidad de la corrección de sodio es variable y difícil de controlar. La solución salina hipertónica también se puede usar en el CSW, con la precaución adicional de evitar la depleción de volumen. Para los pacientes con CSW, el ClNa al 1,5% puede ser más seguro, especialmente si el síndrome es secundario a una hemorragia subaracnoidea, para disminuir el riesgo de depleción de volumen. Sin embargo, es raro el uso de la solución salina hipertónica en los pacientes con CSW.
Furosemida
Este diurético de asa ha sido utilizado en el SIADH para favorecer la excreción del exceso de agua. Bloquea la absorción de sodio y cloro en los riñones, lo que resulta en la excreción de sodio, cloruro y agua. Se ha demostrado que en el SIDADH, la furosemida combinada con el aporte de electrolitos aumenta rápidamente los valores de sodio sérico. Esta corrección rápida es especialmente útil en los pacientes con hiponatremia aguda. En el SIADH, la furosemida debe ser estrechamente monitoreada hasta alcanzar un equilibrio entre la furosemida y la ingesta de sal. Si el equilibrio se desplaza mucho en cualquier dirección, el paciente puede estar en riesgo de deshidratación o sobrecarga de líquido.
Demeclociclina
La demeclociclina puede usarse como tratamiento para el SIADH y también ha sido usada en el SIADH crónico, con el fin de mantener la normalidad de la natremia a largo pazo. La demeclociclina es un antibiótico tetraciclina que en casi el 60% de los pacientes con SIADH actúa induciendo una diabetes insípida nefrogénica. La diabetes insípida es una condición caracterizada por la disminución de la respuesta a la ADH, la excreción de agua y la insuficiencia del riñón para concentrar la orina. La demeclociclina causa diabetes insípida debido al bloqueo de los receptores de vasopresina (ADH) en el riñón. Está disponible por vía oral y en el SIADH se administra en dosis de 600 a 1.200 mg diarios, dividas. El efecto de este fármaco es relativamente impredecible, actúa en menos de los dos tercios de los pacientes, y usualmente su acción comienza a los 2 a 5 días de tratamiento. También puede producir uremia y nefrotoxicidad, en especial en los pacientes con insuficiencia hepática y cirrosis, y fotosensibilidad importante.
Litio
Clásicamente, el litio ha sido utilizado por vía oral para el tratamiento del SIADH. Actúa del mismo modo que la demeclociclina causando diabetes insípida nefrogénica pero es aún menos predecible que ella, actuando solo en el 30% de los pacientes. Se administra por vía oral en dosis de 900 mg/día. Un estudio pequeño de 10 pacientes con SIADH crónico que no corrigieron el problema a pesar de la restricción de agua, comparó el litio con la demeclociclina y comprobó la superioridad de esta última, tanto en eficacia como en seguridad. Los efectos adversos del litio limitan enormemente su uso, entre ellos, provoca trastornos del sistema nervioso central como la pérdida de memoria, síntomas extrapiramidales y miastenia grave. También puede causar temblor, problemas cardíacos, trastornos electrolíticos, nefrotoxicidad, hipotiroidismo, leucocitosis, ganancia de peso, vómitos, diarrea y muchos otros efectos adversos.
Urea
La urea es un diurético osmótico que se ha usado en el SIADH por su capacidad para aumentar la excreción de agua por los riñones. También disminuye la excreción de sodio y ayuda a corregir el estado hipotónico asociado a dicho síndrome. Para el tratamiento del SIADH, el polvo de urea se puede administrar por vía oral, en dosis de 30 g/día, disuelto en agua o una bebida saborizada para mejorar el gusto. En algunos pacientes, la urea no es completamente efectiva para mantener la normalidad del sodio y el balance de agua, pero los pacientes con SIADH pueden mantener un nivel de sodio aceptable con una restricción de líquido más liberal. Los efectos adversos de la urea son las náuseas, los vómitos, la cefalea, la desorientación y la uremia.
Fludrocortisona
La fludrocortisona es un esteroide que aumenta la absorción de sodio en los riñones y su acción ha sido estudiada en la hiponatremia. En un estudio de pacientes con hemorragia subaracnoidea, la fludrocortisona fue administrada para prevenir le depleción de sodio y mantener el estado euvolémico. Un estudio aleatorizado comparó a sujetos tratados con 200 mcg de fludrocortisona, 2 veces por día por vía oral o intravenosa, con placebo. La fludrocortisona fue significativamente más efectiva que el placebo para mantener un balance de sodio negativo durante los primeros 6 días y los 12 días de tratamiento. Los efectos adversos incluyeron el edema pulmonar, la hipopotasemia y la hiperglucemia. En EE. UU. Está disponible en formulación oral. Puede ser efectiva en el CSW, pero su uso está limitado por los efectos adversos.
Antagonistas de la vasopresina
Los antagonistas de los receptores de vasopresina V2 son medicamentos nuevos muy efectivos para el tratamiento de la hiponatremia. Los 2 medicamentos disponibles actualmente en EE. UU. son el conivaptan y el tolvaptan, los que actúan uniéndose a los receptores V2 en el riñón y bloqueando así la ADH. Este proceso causa la excreción de agua libre, por lo tanto, estos fármacos son denominados acuaréticos. Ambos agentes han sido estudiados en el SIADH, destacando que el tolvaptan está disponible para ser usado por vía oral y el conivaptan por vía intravenosa. Otra diferencia es que el conivaptan también bloquea el receptor V1, localizado en la vasculatura y puede causar hipotensión, aunque la importancia clínica de este efecto no ha sido determinada en relación con el aumento del nivel de sodio en los pacientes con SIADH. El tolvaptan se administra por vía oral en dosis de 15, 30 o 60 mg/día, dependiendo de la natremia. Los efectos adversos del tolvaptan son la constipación, la sequedad bucal y el aumento de la micción. El conivaptan se administra en dosis de 20 mg en bolo intravenoso durante 30 minutos, seguido de una infusión continua de 20 a 40 mg/día, hasta 96 horas. Los efectos adversos principales del conivaptan son las reacciones en el sitio de la infusión, el edema, la hipopotasemia, el aumento de la diuresis y de la sed. Los antagonistas de la vasopresina no deben usarse en los pacientes con sospecha de CSW.
Conclusión
La hiponatremia es una anormalidad electrolítica común en UTI y puede ser una causa importante de morbilidad y mortalidad. El manejo del SIADH y el CSW en la UTI puede ser difícil, desde el diagnóstico diferencial entre ambos síndromes hasta el tratamiento, contándose con poca evidencia que oriente acerca de cuál es la mejor estrategia terapéutica. La estrategia terapéutica principal para el CSW sigue siendo el aporte de líquidos isotónicos y de sodio. La evidencia actual indica que la solución salina hipertónica y los antagonistas de la vasopresina pueden ser los tratamientos más efectivos para el SIADH en la UTI. Se requieren más estudios para determinar el tratamiento óptimo de la hiponatremia en los pacientes gravemente enfermos.
♦ Traducción y resumen objetivo: Dra. Marta Papponetti