Introducción
La embolia pulmonar aguda no resuelta es la causa más frecuente de HPTEC
La hipertensión pulmonar tromboembólica crónica (HPTEC) es el aumento de la presión media de la arteria pulmonar a por lo menos 25 mm Hg en reposo. Es causada por la obstrucción persistente de las arterias pulmonares tras una embolia pulmonar a pesar de un mínimo de 3 meses de anticoagulación terapéutica.
Ocasionalmente los pacientes llegan a la consulta con las características clínicas y diagnósticas de HPTEC, incluida la obstrucción de las arterias pulmonares, pero sin hipertensión pulmonar. Formalmente, esto no se debe clasificar como HPTEC, sino como enfermedad tromboembólica crónica, aunque el tratamiento es en general similar al de los pacientes con HPTEC clásica.
La embolia pulmonar aguda no resuelta es la causa más frecuente de HPTEC y se puede producir tras uno o múltiples episodios.
La HPTEC está subdiagnosticada y esto es problemático porque muchos de estos pacientes podrían ser tratados con endarterectomía pulmonar quirúrgica (EAP). Para aquellos que no son candidatos a cirugía, hay tratamientos médicos e intervencionistas y centros especializados que pueden ofrecer tratamientos personalizados para casi todos los pacientes.
Epidemiología, evolución espontánea y patogenia
La resolución incompleta de la embolia pulmonar no es rara. A pesar deI tratamiento anticoagulante eficaz, más del 50% de los pacientes tienen defectos de perfusión residuales 6 meses después del diagnóstico de embolia pulmonar. Sin embargo, la mayoría de estos pacientes no sufren hipertensión pulmonar crónica.
Incluso es improbable que pacientes que tienen signos de hipertensión pulmonar durante un episodio de embolia pulmonar aguda sufran HPTEC y en la mayoría de ellos el ecocardiograma muestra recuperación total de la función ventricular derecha dentro de las 6 semanas. No obstante, algunos pacientes consultan con hipertensión pulmonar persistente y otros sufren hipertensión pulmonar tras un intervalo asintomático de varios meses a varios años.
Se debe tener en cuenta que la hipertensión pulmonar importante no es una característica de la embolia pulmonar aguda, ya que el ventrículo derecho no adaptado no puede generar altas presiones. Por eso cuando los pacientes llegan a la consulta con aparente embolia pulmonar aguda y signos de hipertensión pulmonar grave, es probable que ya sufrieran HPTEC.
La prevalencia estimada de HPTEC tras la embolia pulmonar aguda es del 0,1-4,0% tras 2 años. El riesgo es mayor en pacientes que sufren tromboembolia recidivante, grandes defectos de perfusión y signos ecocardiográficos de hipertensión pulmonar en la consulta inicial.
La aparición de HPTEC no se asocia con los factores de riesgo comunes de tromboembolia venosa, como el factor V Leiden, la mutación del factor II, o una mutación del gen de la protrombina 20210G-A. Una excepción importante es la presencia de anticuerpos antifosfolipídicos, que predisponen a los pacientes a la tromboembolia venosa aguda y a la HPTEC.
Se consideran también factores de riesgo los trastornos mieloproliferativos, la esplenectomía, la enteropatía inflamatoria, la osteomielitis crónica y las líneas venosas permanentes, los marcapasos o las derivaciones ventriculoauriculares.
Estos trastornos se asocian con inflamación crónica, mayor riesgo de sepsis recurrentes o ambas, lo que probablemente contribuye a la no disolución del material tromboembólico. Además, la infección directa del material trombótico por los gérmenes sanguíneos también podría ser importante, especialmente en pacientes con líneas venosas permanentes, marcapasos o derivaciones ventriculoauriculares.
Los mecanismos que impiden la disolución completa del material tromboembólico no se conocen en su totalidad. En general, la resolución de los grandes coágulos se produce en dos pasos, primero la fibrinólisis rápida y después una respuesta celular que conduce a la proliferación de monocitos y células progenitoras endoteliales e inicia la neovascularización del trombo.
Como el proceso puede sufrir alteraciones en cualquiera de estos pasos, los factores que predisponen a la HPTEC varían según las personas. Sobre la base de datos experimentales y el análisis de muestras obtenidas de EAC, varios grupos propusieron un proceso de remodelado vascular alterado, con defectos de la angiogénesis y retardo de la resolución del trombo, junto con disfunción endotelial, como el mecanismo clave dela aparición de HPTEC.
La mediana de supervivencia es de menos de 2 años en aquellos con presión pulmonar mayor de 30 mm Hg
La oclusión de las arterias pulmonares por material tromboembólico es el disparador inicial de la HPTEC. La falta de disolución de este material a la larga produce la formación de tejido cicatrizal organizado, como coágulos fibrosos y membranas y bridas intraluminales, que obstruyen total o parcialmente las arterias pulmonares.
Como consecuencia, el flujo sanguíneo pulmonar se redistribuye a los vasos no ocluidos, que quedan expuestos a altas presiones intravasculares y estrés de cizallamiento, lo que produce disfunción endotelial y remodelado vascular de las arterias precapilares. Estos cambios microvasculares explican por qué la HPTEC es una enfermedad progresiva, aún en ausencia de episodios tromboembólicos recurrentes.
Sin tratamiento, el pronóstico de los pacientes con HPTEC es muy grave. La mediana de supervivencia es de menos de 2 años en aquellos con presión pulmonar mayor de 30 mm Hg. La causa más frecuente de muerte es la insuficiencia cardíaca derecha. Los adelantos terapéuticos mejoraron el pronóstico, pero la HPTEC sigue siendo potencialmente mortal, especialmente cuando la cirugía no es una opción.
Síntomas y diagnóstico
 La disnea de esfuerzo progresiva es el síntoma predominante de la HPTEC. Los pacientes también pueden sufrir fatiga, síncope, hemoptisis y signos de insuficiencia cardíaca derecha. Se debe tener en cuenta la HPTEC en todos aquellos con antecedentes de embolia pulmonar aguda, aunque alrededor del 25% de los pacientes con diagnóstico de HPTEC no tienen antecedentes de embolia pulmonar.
La disnea de esfuerzo progresiva es el síntoma predominante de la HPTEC. Los pacientes también pueden sufrir fatiga, síncope, hemoptisis y signos de insuficiencia cardíaca derecha. Se debe tener en cuenta la HPTEC en todos aquellos con antecedentes de embolia pulmonar aguda, aunque alrededor del 25% de los pacientes con diagnóstico de HPTEC no tienen antecedentes de embolia pulmonar.
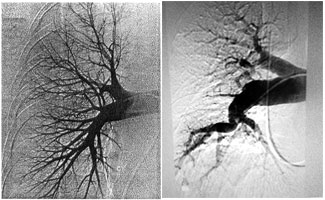
El primer paso diagnóstico es el ecocardiograma transtorácico, para evaluar la probabilidad de hipertensión pulmonar, seguido por una gammagrafía de ventilación perfusión para detectar o descartar defectos de perfusión. Este estudio es el preferido debido a su gran sensibilidad y su valor pronóstico negativo de prácticamente el 100%. Si la gammagrafía es normal se descarta la HPTEC. Los defectos múltiples de perfusión sugieren HPTEC, aunque pueden aparecer también en la enfermedad venosa oclusiva, la vasculitis pulmonar, la mediastinitis fibrosante o los tumores malignos.
La arteriografía por TC multidetector habitualmente revela signos de HPTEC indirectos (patrón en mosaico del parénquima pulmonar y dilatación de las arterias bronquiales) y directos (émbolos organizados, defectos parciales de llenado u obstrucción total de las arterias pulmonares y bridas y membranas. Hallazgos similares se pueden ver en pacientes con trombos no embólicos, tumores o vasculitis de las arterias pulmonares.
Si los estudios por imágenes sugieren una HPTEC será necesario derivar a los pacientes a un centro especializado para más evaluaciones, entre ellas cateterismo del corazón derecho y arteriografía pulmonar.
Se discute si se debe controlar sistemáticamente a los supervivientes de una embolia pulmonar aguda a fin de detectar el surgimiento de HPTEC en una etapa temprana. No se recomienda la pesquisa general tras una embolia pulmonar aguda dado el riesgo bajo, si bien importante, de que aparezca una HPTEC. El umbral para efectuar los estudios diagnósticos, sin embargo, debe ser bajo en pacientes que continúan sintomáticos tras un episodio de embolia pulmonar aguda.
El ecocardiograma sigue siendo la herramienta diagnóstica preferida si se sospecha hipertensión pulmonar, pero el enfoque diagnóstico que combina la ausencia de características de sobrecarga ventricular derecha en el electrocardiograma con concentraciones plasmáticas normales del fragmento N-terminal del propéptido natriurético cerebral tiene un valor pronóstico negativo del 99% para HPTEC.
Tratamiento
Aunque nunca se evaluó en estudios clínicos, la necesidad de anticoagulación de por vida de los pacientes con HPTEC es indiscutible. El índice internacional normalizado deseable es 2,0–3,0. Los antagonistas de la vitamina K son los más empleados. También son adecuadas las heparinas de bajo peso molecular o el fonda parinux.
Los filtros en la vena cava inferior antes se empleaban regularmente, en especial después de la EAP. Ahora cada vez más se emplean sólo cuando la anticoagulación terapéutica no es factible o frente a tromboembolias venosas recidivantes a pesar de suficiente anticoagulación. No hay estudios prospectivos, pero la presencia o la ausencia de filtros de la vena cava no tuvo efecto sobre la supervivencia a 1 año tras la EAP en el registro de HPTEC de la Asociación Internacional de HPTEC (International CTEPH Association).
Endarterectomía pulmonar
Sólo en muy pocos centros se efectúan más de 20 operaciones de EAP por año. La EAP es casi siempre bilateral, lo que implica anestesia general, derivación cardiopulmonar e hipotermia profunda (20°C), porque se necesitan episodios de paro circulatorio total para prevenir el flujo de sangre en el campo quirúrgico. Las arterias pulmonares se abren dentro del pericardio, desde donde se efectúa la endarterectomía lo más distal posible, más allá de las arterias segmentarias y subsegmentarias.
La relación entre la experiencia de cada centro y la tasa de mortalidad es evidente. En los centros con alto volumen de pacientes la mortalidad intrahospitalaria es menor del 5%. La función cognitiva habitualmente no se afecta tras la cirugía a pesar del paro circulatorio periódico y el procedimiento se puede efectuar con riesgos aceptables en pacientes muy ancianos. Además, es posible combinar la EAP con otras operaciones cardíacas.
La hemodinamia posoperatoria es normal o casi normal en la mayoría de los pacientes tras la EAP.
La hipertensión pulmonar residual o recidivante tras la cirugía sigue siendo la causa más importante de morbimortalidad posoperatoria. En el International CTEPH Registry, 64 (16,7%) de 384 pacientes tuvieron hipertensión pulmonar persistente al término de los cuidados intensivos. Skoro-Sajer y colegas informaron hipertensión pulmonar persistente en 14 (31%) de 45 pacientes un año después de la cirugía.
En el único estudio a largo plazo sobre la hemodinamia tras la EAC, Corsico y colegas observaron hipertensión pulmonar persistente en 12 (24%) de 49 pacientes. Estos datos sugieren que la hipertensión pulmonar persistente o recidivante puede ser un problema a tener en cuenta, especialmente en pacientes que llegan a la consulta con disnea progresiva, signos de insuficiencia cardíaca derecha o ambos.
Tratamiento médico
El tratamiento médico de la HPTEC ha sido muy estudiado. Diversas series de casos y estudios no controlados sugirieron inicialmente los efectos favorables de los antagonistas de los receptores de endotelina, los inhibidores de la fosfodiesterasa tipo 5 y los análogos de la prostaciclina. Sin embargo, estudios aleatorizados controlados no tuvieron buenos resultados.
El sildenafil es probablemente el fármaco más empleado para tratar a pacientes con HPTEC inoperable, pero sólo hay un estudio aleatorizado controlado de este fármaco, que no mostró cambios en prueba de caminata de 6 minutos, pero se asoció con mejoría significativa de la clase funcional y la hemodinamia. Estos resultados, no obstante, se basaron sobre sólo 17 casos, es decir que el estudio carece de poder estadístico.
El primer gran estudio aleatorizado, doble ciego, controlado en este campo fue el BENEFiT, que evaluó la seguridad y la eficacia de 16 semanas de tratamiento con bosentán, antagonista del receptor de endotelina, versus placebo en pacientes con HPTEC inoperable o persistente o hipertensión pulmonar recidivante tras la EAP. La resistencia vascular pulmonar mejoró significativamente, pero no mejoraron la prueba de caminata de 6 minutos ni otros parámetros clínicos.
A pesar de estos resultados, las recomendaciones para la hipertensión pulmonar aconsejan el empleo cauteloso de antagonistas del receptor de endotelina, inhibidores de la fosfodiesterasa tipo 5 y análogos de la prostaciclina en pacientes con HPTEC inoperable. Faltaría confirmar los beneficios de estos tratamientos mediante estudios aleatorizados prospectivos.
En 2013, el riociguat se convirtió en el primer fármaco autorizado para el tratamiento de la HPTEC inoperable, incluida su persistencia o recurrencia tras la EAP. El riociguat estimula la actividad de la guanilato ciclasa soluble, con lo que ejerce efectos vasodilatadores y antiproliferativos sobre las células del músculo liso vascular. En un estudio no controlado de fase 2, el riociguat tuvo efectos similares sobre la hemodinamia y la capacidad de ejercicio en pacientes con HPTEC y en aquéllos con hipertensión pulmonar.
El estudio ulterior de fase 3, CHEST-1, confirmó los datos del estudio en fase 2. Riociguat se asoció con mejoras significativas de la prueba de caminata de 6 minutos, la resistencia vascular pulmonar, la clase funcional y las concentraciones del fragmento N-terminal del propéptido natriurético cerebral después de 16 semanas de tratamiento.
El fármaco fue bien tolerado, con algunos efectos colaterales. Nuevos estudios proporcionarán más información sobre su seguridad. La autorización del riociguat para pacientes con HPTEC inoperable cierra una brecha terapéutica importante, pero al mismo tiempo agrava otra cuestión: la de recetar medicamentos en pacientes con HPTEC en lugar de derivarlos a un centro especializado para evaluación de posibles procedimientos diagnósticos invasivos y la perspectiva de cirugía mayor.
Se debe tener presente que la cirugía es la única opción curativa para la HPTEC. La utilidad del tratamiento médico se demostró sólo en pacientes con enfermedad realmente inoperable. Por ello, la operabilidad o la inoperabilidad deben ser determinadas lo antes posible por equipos especializados multidisciplinarios.
Aunque el tratamiento medicamentoso está autorizado para pacientes con HPTEC inoperable y para pacientes con hipertensión pulmonar persistente o recidivante después de la EAP, la evidencia aún no es robusta para este último grupo.
Se estudió el tratamiento médico para disminuir la resistencia vascular pulmonar antes de la EAP, ya que los valores altos son un factor de riesgo independiente de mortalidad postoperatoria. Varios estudios pequeños mostraron que los fármacos empleados para la hipertensión pulmonar podrían mejorar la hemodinamia en los candidatos a cirugía, pero no hay evidencia que indique mejores resultados posoperatorios.
Ningún dato indica la eficacia del tratamiento médico para pacientes con HPTEC proximal con enfermedad que se considera operable, pero que no se operan debido a graves enfermedades asociadas. A pesar de que en general se excluye a estos pacientes de los estudios aleatorizados controlados, la evidencia de estudios en otros pacientes sugiere que cabría esperar mejoría hemodinámica en esta población.
Angioplastia pulmonar con balón
Una opción terapéutica posible para la HPTEC es la angioplastia pulmonar con balón. A pesar de sus resultados prometedores, esta técnica no fue adoptada ampliamente porque se asoció con complicaciones importantes, posiblemente mortales, especialmente edema de reperfusión y hemorragia pulmonar. Sin embargo, la técnica comenzó a generar interés tras su empleo en varios centros japoneses. Durante cada sesión se trata una sola zona y esto reduce al mínimo el riesgo.
Habitualmente son necesarias de tres a cinco sesiones. El tamaño del balón siempre es menor que el diámetro del vaso porque el objetivo principal no es dilatar, sino reabrir los vasos ocluidos por bridas y membranas. Las principales zonas a tratar son los vasos segmentarios y subsegmentarios. En centros japoneses y europeos se demostraron impresionantes mejorías hemodinámicas, así como en la capacidad de ejercicio, las concentraciones plasmáticas del péptido natriurético cerebral y retroceso del remodelado ventricular derecho.
Se observaron complicaciones graves, incluida hemorragia pulmonar mortal, pero son raras y hay una relación inversa entre las complicaciones importantes y la experiencia de cada centro. La mortalidad periprocedimiento fue del 1,5% en las series más grandes. Durante la observación de hasta 3 años, se observó sólo ocasionalmente restenosis, sin que fuera necesaria la colocación de un stent, pero los resultados alejados se deben evaluar aún más.
La angioplastia pulmonar con balón sigue siendo un procedimiento experimental, con pocos datos a largo plazo. Al igual que el tratamiento médico, la angioplastia pulmonar con balón presenta al mismo tiempo riesgos y oportunidades. Para la HPTEC principal y lobular, la cirugía continúa siendo el tratamiento más eficaz, al igual que cuando se obstruyen totalmente gran número de arterias pulmonares segmentarias o subsegmentarias. Incluso cuando la angioplastia pulmonar con balón es exitosa, con frecuencia persiste hipertensión pulmonar residual y la mayoría de los pacientes reciben también los tratamientos médicos empleados en la hipertensión pulmonar antes y después de la intervención.
La mayoría de los centros importantes de HPTEC y EAP en todo el mundo agregaron la angioplastia pulmonar con balón a sus opciones terapéuticas.
La EAP sigue siendo el tratamiento más eficaz para la HPTEC y en muchos pacientes es el tratamiento definitivo y curativo. La angioplastia pulmonar con balón se podría tener en cuenta para pacientes que se consideran inoperables debido a enfermedad predominantemente distal o a enfermedades asociadas o en aquellos pacientes con hipertensión pulmonar persistente o recurrente después de la EAP.
Conclusiones
La HPTEC es una complicación potencialmente mortal de la embolia pulmonar. El tratamiento es muy diferente al de otras formas de hipertensión pulmonar. Las pruebas diagnósticas necesarias en pacientes con hipertensión pulmonar inexplicada deben comprender estudios por imágenes, entre ellos la gammagrafía de ventilación-perfusión.
El diagnóstico definitivo de HPTEC exige cateterismo del corazón derecho y arteriografía pulmonar, que se deben efectuar en centros especializados, donde se determinará también el mejor enfoque terapéutico. La EAP es el tratamiento de elección y continúa siendo el único enfoque terapéutico que puede ser curativo. Para pacientes con enfermedad inoperable, el riociguat es hasta ahora el único fármaco autorizado que mejora la hemodinamia y la capacidad de ejercicio.
La angioplastia pulmonar con balón es una nueva opción terapéutica para determinados pacientes con enfermedad inoperable, pero exige mayor evaluación antes de que se pueda determinar su lugar en la estrategia terapéutica para la HPTEC.
♦ Traducción y comentario objetivo: Dr. Ricardo Ferreira