El factor de necrosis tumoral (TNF) reduce la replicación del virus de hepatitis B (HBV). Existe evidencia que indica un riesgo de reactivación de HBV o agravamiento en pacientes con infección crónica por hepatitis B al usar agentes anti-TNF.
Existen algunos reportes de hepatitis fulminante durante la terapia biológica.
Recientemente, pocos reportes han sugerido la posible reactivación de HBV en pacientes con antígeno de superficie negativo (HBsAg) luego del tratamiento con agentes biológicos.
El objetivo del estudio fue evaluar la seguridad de los agentes anti-TNF a en pacientes con psoriasis y serología sugestiva de hepatitis B pasada.
Se evaluaron retrospectivamente los resultados de pacientes con psoriasis con serología sugestiva de infección pasada por HBV durante el tratamiento con terapia anti-TNF.
Los criterios de inclusión eran los siguientes: psoriasis en placas moderada a severa tratada con terapia anti TNF en monoterapia por al menos 9 meses. HBsAg negativo y anticuerpo core hepatitis B (HBcAb) positivo.
Se evaluaron 13 pacientes, 4 mujeres y 9 hombres. Los datos basales se encuentran en la tabla 1. La duración media del tratamiento con anti-TNF era de 28.6 meses (9-86 meses). El agente prescripto más comúnmente fue etanercept (siete casos), seguido de infliximab (4 casos) y adalimumab (dos casos). De los 9 pacientes que tenían dos mediciones de HBV basal y al final del seguimiento ninguno positivizó el HBsAg.
Todos los pacientes permanecieron positivos para HBcAb, excepto paciente 9. El título de HBsAb disminuyó en 3 y aumentó en 1 (caso 4) de los 8 pacientes HBsAb positivos al escreening. Los casos 4 y 13 positivizaron HBsAb (tabla 2). Durante el periodo de seguimiento no se encontraron evidencias significativas en los niveles de enzimas hepáticas, excepto en el paciente 10, que presentó incrementos periódicos de la gammaglutamiltranferasa con ecografía normal.
En las guías Europeas del uso de terapia anti-TNF en psoriasis publicadas en el 2009, la hepatitis B crónica activa es una contraindicación absoluta, y no se recomienda tratar a los portadores crónicos de hepatitis B con terapia anti-TNF. Sin embargo, no está resuelto el manejo de pacientes HBsAg negativos. La HBV puede persistir en casos de HBs Ag negativos luego de infección por HBV, con una prevalencia del 6 al 15.3% en países donde la infección es endémica.
Existen escasos reportes de reactivación de HBV luego de transplantes o durante quimioterapia en pacientes con estado serológico que indique infección pasada por HBV.
En la literatura dermatológica, Prignano y col reportaron 11 pacientes con infección pasada HBV y psoriasis tratada con etanercept. Ninguno de los pacientes mostró cambios significativos en las aminotranferasas séricas ni positividad HBsAg, y el ADN HBV permaneció indetectable al final del periodo de seguimiento.
En esta serie ninguno de los pacientes positivizó el HBsAg ni mostró incrementos de las transaminasas. En el caso 9, el HBcAb se negativizó, sugiriendo que la medición basal fue un falso positivo.
No existen criterios diagnósticos uniformes disponibles para definir la reactivación de HBV. Se ha definido como el incremento en la replicación de HBV desde un nivel bajo a alto en pacientes con HBV crónica o pasada. El incremento de enzimas hepáticas puede no ser suficiente para evaluar reactivación, ya que el incremento de los niveles de ADN HBV generalmente precede a la elevación de las enzimas en días o semanas.
El monitoreo de HBsAg puede ser útil para detectar reactivación por HBV, a pesar de algunos casos reportados de reactivación mientras el HBsAg permanece negativo en pacientes tratados con tacrolimus, rituximab o ciclofosfamida. La posibilidad de pacientes HBsAg negativos que desarrollan reactivación HBV es menor que para los pacientes HBsAg positivos. En los pacientes severamente inmunodeprimidos el riesgo de reactivación es mayor, y algunos autores defienden que un enfoque alternativo sería monitorear el ADN HBV y las transaminasas.
Las limitaciones de este estudio incluye escaso número de pacientes y que los datos no estaban completos en todos los pacientes, ya que el monitoreo de HBsAg en pacientes negativos no se recomendaba años atrás.
Basado en la literatura, y a pesar del bajo riesgo de reactivación (según lo observado en este estudio), se recomienda el monitoreo sérico de niveles de aminotranferasas, HBsAb, HBsAg y si fuera possible carga viral en pacientes HBsAg-negativo/HBcAb-positivo durante el tratamiento con terapia anti-TNF.
¿Qué aporta este artículo a la práctica dermatológica?.
Recientemente, se ha descripto excepcionalmente la reactivación durante el tratamiento con bloqueantes del factor de necrosis tumoral en pacientes con hepatitis B (HBV) antígeno negativo (HBsAg). El objetivo del estudio fue evaluar la influencia de los agentes anti TNF en pacientes con psoriasis y serología que sugiere hepatitis B pasada. Los criterios de inclusión fueron psoriasis en placas crónica tratada con terapia anti TNF, HBs Ag negativo y HBcAb positivo. Se incluyeron 13 pacientes. Ninguno de los pacientes positivizó el HBsAg. Se recomienda el monitoreo sérico de aminotranferasas, HBs Ab, HBsAg y si es posible carga viral.
Tabla 1: Características basales de pacientes HBsAg-negativo/HBcAb-positivo.
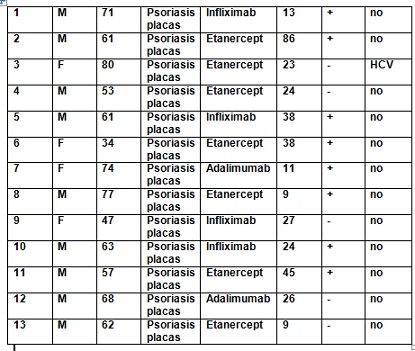
HBcAb, anticuerpo core hepatitis B virus; HBsAb, anticuerpo superficie del virus de hepatitis B; HBsAg, antigeno de superficie de hepatitis B; HCV, infección por virus de hepatitis C virus
Tabla 2: Evolución del título de anticuerpo de superficie de hepatitis B y de enzimas hepáticas durante el periodo de seguimiento.
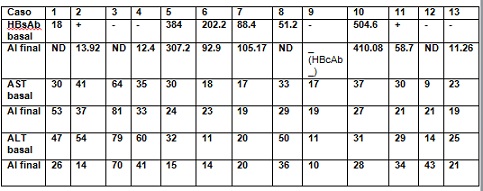
negativo; +, positivo; ALT, alanino aminotransferasa; AST, aspartato aminotransferasa; HBcAb, anticuerpo core hepatitis; HBsAb, anticuerpo de superficie virus hepatitis B virus; ND, no determinado.
Comentario y resúmen objetivo: Dra. Geraldina Rodríguez Rivello