La terapia con insulina es una de las herramientas médicas más eficaces que pueden usarse para ayudar a los pacientes a alcanzar su hemoglobina glicosilada (HbA1c) objetivo. Sin embargo, las decisiones sobre cuándo y cómo iniciar la terapia con insulina tienen que ser individualizadas y adaptadas a las necesidades y objetivos de cada paciente. Existen muchas opciones de terapia con insulina; una de las más comunes es el agregado de insulina basal a los medicamentos antidiabéticos orales. A pesar de que los pacientes suelen ser reacios a iniciar la terapia con insulina, esta resistencia puede ser superada a través de la educación y el entrenamiento del paciente.
Eventualmente, la mayoría de los pacientes necesitan insulina
La diabetes mellitus tipo 2 (DM2) es una enfermedad crónica progresiva asociada con la resistencia a la insulina, la disfunción de las células ß y la disminución de la secreción de insulina. En consecuencia, con el tiempo, la mayoría de los pacientes requiere la terapia con insulina para reducir el riesgo de complicaciones a largo plazo.
La eficacia de esta terapia puede ser evaluada mediante la medición de la HbA1c, un marcador importante del estado hiperglucémico crónico. El valor de la HbA1c puede ser reportado como una relación (%) estandarizada con los resultados del Diabetes Control and Complications Trial o como unidades de la International Federation of Clinical Chemistry (mmol/mol). Debido a que la DM2 es una enfermedad progresiva, la mayoría de los pacientes finalmente necesita insulina.
|
Puntos clave
|
¿Cuál es la HbA1C apropiada?
La respuesta corta es: "depende".
Actualmente, la American Association of Clinical Endocrinologists (AACE) apoya una HbA1c objetivo <6,5% para los pacientes por lo demás sanos, pero afirma que el objetivo debe ser individualizado para los pacientes con enfermedades concurrente o en riesgo de hipoglucemia.
Por otro lado, para la mayoría de los adultos con DM2, la American Diabetes Association (ADA) recomienda un valor objetivo de la HbA1c más elevado (<7%). Se demostró que se asocia con una reducción de las complicaciones micro y macrovasculares de la diabetes. Sin embargo, cuando recientemente 3 grandes estudios hicieron la comparación entre el control de la glucosa intensivo y estándar, el control más estricto no mejoró los resultados cardiovasculares. Por otra parte, en uno de los ensayos, 7 pacientes que habían recibido tratamiento intensivo tuvieron una tasa de mortalidad global más elevada.
Detalles:
• Action in Diabetes and Vascular Disease (AVANCE): 11.140 pacientes; niveles promedio de HbA1c 6,5% vs. 7,3%
• Action to Control Cardiovascular Risk in Diabetes (ACCORD): 10.251 pacientes; niveles promedio de HbA1c 6,4% vs. 7,5%
• Veterans Affairs Diabetes Trial (VADT (VADT): 1.791 pacientes; niveles promedio de HbvA1c de 6,9% vs. 8,4%.
Del mismo modo, una revisión de Cochrane de 2013 que incluyó 28 ensayos controlados y aleatorizados llegó a la conclusión que el control intensivo (18.717 pacientes) no disminuye las tasas de mortalidad global y cardiovascular comparado con el control tradicional de la glucosa (16.195 pacientes); también se observó un aumentó del riesgo de hipoglucemia y eventos adversos graves.
Como resultado, la ADA establece que una HbA1c objetivo <6,5% es una opción para los pacientes con una esperanza de vida larga y una diabetes de poca antigüedad, una riesgo bajo de hipoglucemia y sin enfermedad cardiovascular significativa. Por otra parte, la ADA propone un objetivo de HbA1c <8% para los pacientes con antecedentes de hipoglucemia grave, esperanza de vida limitada, complicaciones micro o macrovasculares avanzadas, amplias condiciones comórbidas y DM de larga data. Por lo tanto, la AACE y la ADA se apartan bastante del objetivo de "una sola medida para todos", individualizando sus recomendaciones.
¿Cuándo se debe iniciar la insulina?
Los médicos deben tener en cuenta las necesidades y preferencias de cada paciente e individualizar el tratamiento. La recomendación más reciente de la ADA hace hincapié en la importancia de un enfoque centrado en el paciente, y la consideración de múltiples factores. Estos incluyen la actitud del paciente en cuanto al cumplimiento del tratamiento, el riesgo de hipoglucemia, la duración de la enfermedad, la expectativa de vida, las comorbilidades y los efectos secundarios de los medicamentos orales y la insulina.
En comparación con las guías previas, hay menos reglas sobre cómo y cuándo comenzar la terapia con insulina. Pero en los pacientes que se mencionan a continuación, deben considerarse tanto las indicaciones absolutas como las relativas.
Indicaciones absolutas para la insulina
• Cetoacidosis o síntomas catabólicos, incluyendo la cetonuria.
• DM2 recién diagnosticada, con pronunciada hiperglucemia (≥300 mg/dl o una HBA1c ≥10,0%) con o sin síntomas graves, incluyendo la pérdida de peso, la poliuria o la polidipsia.
• DM2 no controlada a pesar de utilizar 1, 2 o más fármacos antidiabéticos orales o los agonistas de los receptores del péptido símil glucagón 1 (GLP-1).
• Diabetes gestacional.
• Preferencia por la insulina.
Indicaciones relativas para la insulina
• Paciente hospitalizado por cirugía o enfermedad aguda.
• Enfermedad renal o hepática avanzada.
• Incapacidad para afrontar el costo de la insulina o para tolerar los efectos secundarios de los medicamentos antidiabéticos orales y los agonistas de los receptores del GLP-1. Dependiendo de la situación, la glucemia se mide en ayunas, antes de las comidas, o después de las comidas o después de iniciar o ajustar los regímenes de insulina.
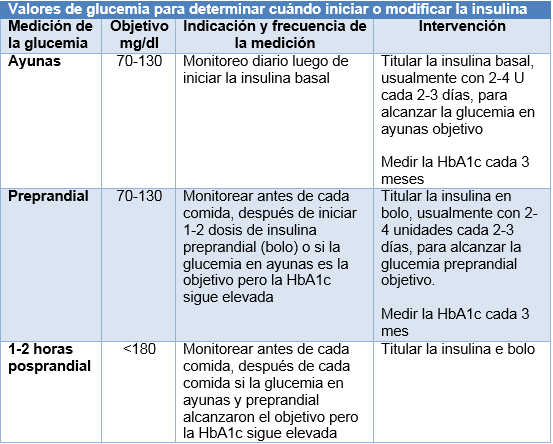
¿Cuáles son los regímenes de insulina?
Insulina basal
En las primeras etapas de la DM2, se utiliza la metformina sola o combinada con otro antidiabético oral o un agonista del receptor del GLP-1, junto con una alimentación saludable, control de peso y aumento de la actividad física.
Cuando la HbA1c objetivo no se puede lograr con 1 o 2 fármacos no insulínicos, la ADA recomienda agregar insulina basal a un régimen de la metformina o de 2 medicamentos, siendo uno de ellos la metformina. Sin embargo, la evidencia reciente indica que la combinación de un agonista del receptor del GLP-1 más insulina basal en un régimen sin metformina, es segura y mejora el control glucémico, sin hipoglucemia o ganancia de peso.
Si bien en los pacientes con una HbA1c <8% inicialmente podría utilizarse una dosis diaria total de insulina de 0,1 a 0,2 U/kg, cuando la HbA1c está entre el 8% y el 10% se requiere una dosis mayor, de 0,2 a 0,3 U/kg. Si la glucemia en ayunas es superior a la nivel objetivo (normalmente <130 mg/dl) puede ajustarse la dosis 1-2 veces/semana. Si aparece hipoglucemia (gluccemia <70 mg/dL) se debe reducir la dosis de insulina un 10-20%.
| Medicamentos que se pueden utilizar con insulina en la DM2 |
|
Primer medicamento |
| Sulfonilureas de segunda generación (preferido) Gliburida Glipizida Glimepirida Meglitinidas * Repaglinida Nateglinida |
| Inhibidores de la dipeptidil peptidasa 4 Sitagliptina Saxagliptina Linagliptina Alogliptina |
| Péptido símil glucagón 1 agonistas Exenatida Liraglutida Exenatida ER Albiglutide Dulaglutide Tiazoldinedionas Rosiglitazona Pioglitazona |
| Inhibidores de α-glucosidasa * Acarbosa Miglitol |
| Inhibidores del cotransportador de sodio-glucosa 2* Canaglifozina Dapagliflozina Empagliflozin |
* Solo mencionados en la guía de la Americana Association of Clinical Endocrinologists
Las insulinas basales disponibles son: glargina, detemir y protamina neutra Hagedorn (NPH). Debido a que la glargina y el detemir tienen mejores propiedades farmacocinéticas la variabilidad de la respuesta es menor con menos riesgo de hipoglucemia, por lo que se las prefiere a la NPH.
La glargina tiene una concentración plasmática relativamente constante durante 24 horas, permitiendo dosificarla 1 vez/día en cualquier momento del día. La dosis debe ser administrada a la misma hora todos los días. En general, el detemir y la NPH se administran 1-2 veces/día. Los pacientes tratados 1vez/día deberían recibir la dosis con la cena o antes de acostarse. Los pacientes que requieren un régimen de 2 veces/día pueden recibir la primera dosis en el desayuno y la segunda con la comida de la noche, antes de acostarse o 12 horas después de la dosis de la mañana.
El ensayo aleatorizado Treat-to-Target en 756 pacientes mostró que tanto la glargina como la NPH, cuando son agregadas a la terapia oral de los pacientes con DM2, alcanzan el objetivo de HbA1c, pero la NPH se asocia con más episodios de hipoglucemia nocturna. Resultados similares se hallaron cuando se comparó la NPH con la insulina detemir.
Una revisión de Cochrane mostró que la glargina y el detemir son similares en eficacia y seguridad. Sin embargo, con frecuencia el detemir necesita ser inyectado 2 veces/día, en una dosis más elevada y se asocia con un menor aumento de peso. Por otra parte, un metaanálisis de 46 ensayos clínicos aleatorizados mostró que el aumento de peso a 1 año es menor en los pacientes tratados con regímenes basales que con regímenes de 2 veces/día o prandiales.
Un estudio longitudinal de no intervención de 2.179 pacientes que habían iniciado recientemente la terapia con insulina mostró que el aumento de peso promedio al año fue de 1,78 kg, mientras que el 24% de los pacientes aumentó >5 kg. Sin embargo, los factores que se asociaron en forma independiente al aumento de peso fueron una HbA1c basal más elevada, dosis más elevada de insulina basal y al año y un índice de masa corporal inicial menor, y no el régimen de insulina utilizado.
Actualmente se está estudiando una nueva clase de insulina basal de acción ultra larga. Las insulinas de esta clase están aprobados en otros países, pero para su aprobación, la Food and Drug Administration requiere datos adicionales. Se espera que las insulinas de acción ultra larga reduzcan el riesgo de hipoglucemia, específicamente el riesgo de episodios nocturnos. Por otra parte, dada la acción más prolongada y una farmacocinética en equilibrio estable, estas insulinas permitirán ser flexibles en la dosificación.
Regímenes con bolo basal
En general, la insulina basal no controla la hiperglucemia postprandial. Las glucemias postprandiales mayores al valor objetivo (por lo general>180 mg/dL) o una HbA1c previa superior al valor objetivo a pesar de una glucemia en ayunas bien controlada obliga a administrar dosis de insulina múltiples (incluyendo ≥1 dosis preprandiales). Esto se hace evidente cuando la dosis diaria total de insulina basal excede las 0,5 U/kg. Los pacientes recién diagnosticados con DM que tienen una HbA1c <10% también pueden responder mejor a un régimen inicial basal en bolo.
Los bolos de Insulinas disponibles incluyen las insulinas lispro, aspart, glulisina, la insulina regular y la nueva insulina regular inhalada recientemente aprobada Technosphere. Pueden administrarse antes de cada comida y la dosis total del bolo en general representa el 50% de la dosis total diaria. Las insulinas de acción rápida tienen un inicio más rápido, son de duración más corta y tienen una farmacocinética más previsible, lo que las hace preferibles a la insulina regular.
La insulina inhalada es otra opción, pero está contraindicada en los pacientes con enfermedad pulmonar obstructiva crónica o asma, debido al mayor riesgo de broncoespasmo agudo. Por otra parte, la transición a un régimen con bolo basal se puede lograr con una sola dosis de insulina antes de la comida principal, utilizando una dosis que representa aproximadamente el 10% de la dosis diaria total.

Dosis adicionales en bolo
Las dosis en bolo adicionales se pueden agregar más adelante sobre la base del control glucémico. El ajuste de la dosis de insulina preprandial se realiza 1-2 veces/semana, basado en los valores de la glucemia postprandial.
Para los pacientes que no pueden cumplir con un régimen de insulina complejo se pueden considerar las combinaciones premezcladas de insulinas de acción prolongada y corta, que proporcionan una mezcla de 50% y 50%, 70% y 30% o 75% y 25%. Una comparación prospectiva de diferentes regímenes de insulina (basal, premezclada, a la hora de comer más basal y, a la hora de la cena) en pacientes con DM2 reveló que la reducción de la HbA1c fue similar en los diferentes grupos. Sin embargo, el número de episodios de hipoglucemia fue superior en el grupo de insulina premezclada, y la ganancia de peso fue menor en el grupo de insulina basal.
Si bien las insulinas premezcladas requieren menos inyecciones no brindan flexibilidad de dosificación. Es decir, los ajustes de dosis para las insulinas premezcladas conducen a un aumento tanto de las dosis basales como de los bolos, a pesar de que es necesario ajustar la dosis de un solo tipo de insulina. Por lo tanto, ésta es una razón habitual del aumento de los episodios de hipoglucemia.
Infusión continua de insulina subcutánea
Un metaanálisis mostró que la infusión de insulina sucutánea continua (es decir, el uso de una bomba de insulina) fue similar a la terapia intensiva con múltiples inyecciones de insulina diarias en términos del control de la glucemia y la hipoglucemia. Dado que ambas opciones pueden conducir a un control similar de la glucosa, al iniciar la infusión de insulina se deben tener en cuenta los factores adicionales a, como el estilo de vida y los conocimientos técnicos. Algunos pacientes pueden no preferir estar unidos a una bomba durante casi todas las actividades diarias. Por otra parte, este tipo de terapia es compleja y requiere un gran entrenamiento para garantizar la eficacia y seguridad.
¿Cuál es el costo de la terapia con insulina?
Un último factor a tener en cuenta al iniciar la terapia con insulina es el costo. Es importante informarse de cuál es el formulario de prescripción de su seguro médico para asegurarse de que la prescripción elegida tiene un costo asequible para el paciente. Si los pacientes no tienen un seguro que cubra su tratamiento, una opción es recurrir a los programas de provisión de medicamentos. Sin embargo, si un paciente acepta la bomba de insulina, es esencial la cobertura del seguro médico. Dependiendo del fabricante, las bombas de insulina cuestan alrededor de $6.000 a $7.000, y el suministros mensual adicional para la bomba también es costoso. Si los pacientes se comprometen a seguir un tratamiento con insulina, la probabilidad de éxito del tratamiento es mayor.
Traducción y resumen objetivo: Dra. Marta Papponetti