| Introducción |
Mavacamten es el primer y único inhibidor de la miosina cardíaca aprobado a nivel mundial para el tratamiento de adultos con miocardiopatía hipertrófica (MH) obstructiva sintomática de clase II-III de la New York Heart Association (NYHA).
En el ensayo para aprobación del fármaco, aleatorizado y de fase 3, llamado EXPLORER-HCM (NCT03470545), se demostró que mavacamten fue superior al placebo para lograr mejoras en las medidas clínicas, los síntomas y los resultados informados por los pacientes con MH obstructiva, durante 30 semanas. Además, los pacientes que completaron el EXPLORER-HCM pudieron inscribirse en la cohorte EXPLORER del estudio MAVA-LTE (NCT03723655), después de un período de lavado de 8 semanas.
El objetivo fue presentar los datos de seguridad y eficacia a largo plazo hasta la fecha de la cohorte EXPLORER de MAVA-LTE, hasta la semana 180, inclusive (finalización de la recopilación de datos: 31 de agosto de 2024).
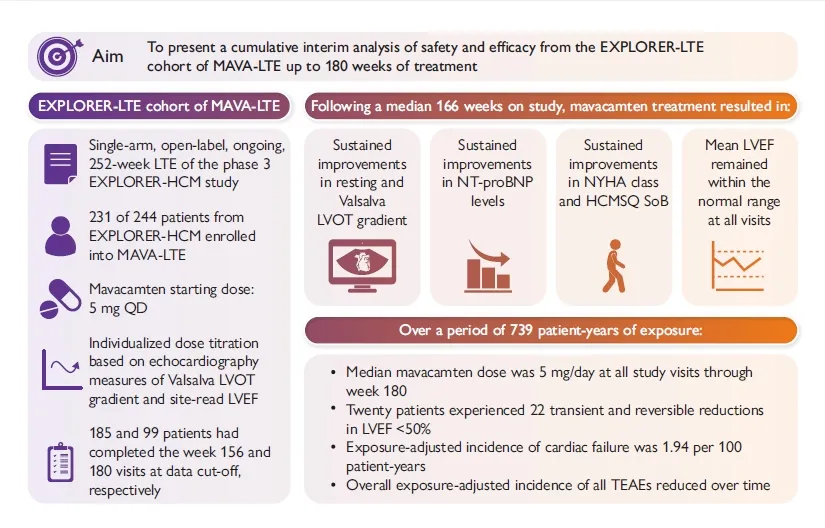
Resumen gráfico estructurado. Dosis inicial de mavacamten: 5 mg, una vez al día. Titulación de dosis individualizada, basada en mediciones ecocardiográficas del gradiente de Valsalva en el LVOT y la FEVI.
| Diseño del estudio |
Después de la titulación, los pacientes se evaluaron a intervalos de 12 semanas, entre las semanas 24 y 156. La semana 180 fue la primera visita después de un intervalo de 24 semanas.
Mavacamten se suspendió temporalmente si la fracción de eyección del ventrículo izquierdo (FEVI) leída en el sitio estaba < 50 % en cualquier visita. Los pacientes podían reanudar el tratamiento a un nivel de una dosis inferior a la dosis anterior, si la FEVI era ≥ 50 % en la visita de seguimiento, 4-6 semanas después.
| Resumen del ensayo MAVA-LTE |
El estudio a largo plazo MAVA-LTE evaluó la seguridad y eficacia de mavacamten en pacientes con MH. Este ensayo clínico, que fue una extensión de 5 años del estudio EXPLORER-HCM, investigó los efectos prolongados de este inhibidor de la miosina cardíaca. Los participantes del estudio original fueron seguidos durante una mediana de 166 semanas, mostrando mejoras sostenidas en los gradientes del tracto de salida del ventrículo izquierdo (TSVI), la FEVI y los niveles de NT-proBNP, un biomarcador clave para la insuficiencia cardíaca.
Durante el seguimiento, mavacamten demostró ser eficaz en la reducción de los gradientes TSVI, tanto en reposo como durante la maniobra de Valsalva, con una disminución media de 40,3 mmHg y 55,3 mmHg, respectivamente, a la semana 180. Además, se observó una reducción significativa en los niveles de NT-proBNP, indicando un progreso en la presión diastólica del ventrículo izquierdo. Estas mejoras se tradujeron también en una mejora notable en la clase funcional de la NYHA: al final del estudio, más del 77 % de los pacientes habían mejorado al menos un nivel en la clasificación de la NYHA.
En términos de seguridad, mavacamten fue bien tolerado durante el periodo de estudio a largo plazo. Aunque algunos pacientes experimentaron reducciones transitorias en la FEVI, por debajo del 50 %, todos los casos se recuperaron tras la interrupción temporal del tratamiento. En total, el 8,7 % de los pacientes experimentaron estas reducciones, lo cual se traduce en una incidencia ajustada a la exposición de 2,77 eventos por cada 100 años-paciente. Además, no se identificaron nuevas preocupaciones de seguridad a lo largo del estudio. Las muertes que ocurrieron durante el ensayo no fueron relacionadas con el tratamiento de mavacamten, según los investigadores.
El estudio también destaca la estabilidad en la dosificación de mavacamten entre los pacientes a lo largo del tiempo, con la mayoría manteniendo la misma dosis desde la semana 24 hasta la semana 180. Esta estabilidad sugiere que el monitoreo de los gradientes TSVI y la FEVI a través de ecocardiogramas fue suficiente para ajustar la dosis de manera adecuada, sin necesidad de medir las concentraciones plasmáticas de mavacamten o considerar el fenotipo del metabolizador CYP2C19.

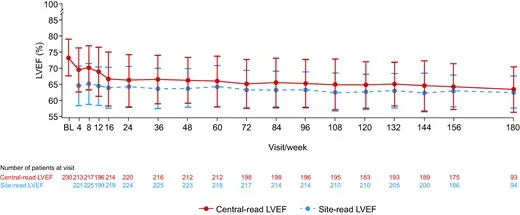
• Las mejoras en los gradientes de reposo y TSVI de Valsalva con el tratamiento con mavacamten se mantuvieron durante las semanas 156 y 180, como lo confirmaron los ecocardiogramas de lectura del sitio y de lectura central.
• En total, 191 pacientes (82,7 %) alcanzaron un gradiente del TSVI de Valsalva de lectura central de ≤ 30 mm Hg, indicativo de ausencia de obstrucción, durante el estudio, y se mantuvieron en o por debajo del umbral de 30 mm Hg hasta el corte de los datos.
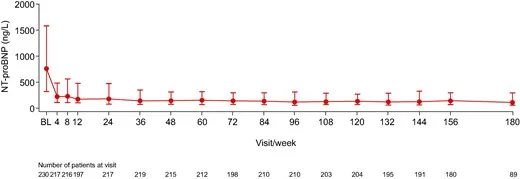
• La proporción de pacientes con una concentración de NT-proBNP < de 124 ng/L, indicativo de un rango normal, aumentó del 9,6 % al inicio del estudio al 43,2 % en la semana 156 y al 53,8 % en la semana 180.
|
Conclusiones El tratamiento a largo plazo con mavacamten, en pacientes con miocardiopatía hipertrófica obstructiva, resultó en mejoras significativas y sostenidas en la función cardíaca, los síntomas y la calidad de vida, manteniendo un perfil de seguridad favorable. Estos hallazgos respaldan el uso continuo de mavacamten como una opción de tratamiento eficaz para mejorar la calidad de vida de los pacientes con MH obstructiva, proporcionando alivio sintomático y mejorando la función cardíaca, sin comprometer la seguridad a largo plazo. |
Nota auspiciada por Bristol Myers Squibb Argentina. CAMZYOS® (mavacamten) es una especialidad medicinal registrada por Bristol Myers Squibb Argentina S.R.L. Certificado ANMAT Nº 59905. Prospecto de Prescripción Vigente. Para acceder al prospecto vigente de CAMZYOS® (mavacamten) aprobado haga click acá: https://www.bms.com/assets/bms/argentina/documents/prospecto/Camzyos-Prospecto.pdf. 3500-AR-2400078.