| Introducción |
El estrés es inducido por una situación difícil o un incidente desafiante conocido como factor estresante, frente al cual el cuerpo desarrolla una respuesta fisiológica o psicológica denominada respuesta al estrés. Cuando el cuerpo está bajo estrés, el sistema inmunitario responde movilizando células específicas en el torrente sanguíneo, lo que ayuda en la lucha o la huida.
Los niveles sanguíneos de citocinas proinflamatorias aumentan durante el estrés, activando así los virus latentes. Selye, el "padre" del estrés, describió las 3 fases del mismo:
- La primera y la segunda fase son reacciones de alarma y resistencia, respectivamente, y no son peligrosas.
- La tercera fase (agotamiento) puede causar deterioro de la salud.
Los linfocitos exhiben receptores adrenérgicos dependientes del estrés que alteran su actividad, debido a la estimulación adrenérgica. Por otra parte, los patrones de conducta están vinculados a las vías de estrés y al sistema inmunitario.
| Descripción general del sistema inmunitario |
El sistema inmunitario es una red altamente intrincada y dinámica responsable de defender al cuerpo contra una amplia gama de patógenos, incluidos bacterias, virus, hongos y parásitos. Se pueden clasificar dos respuestas inmunitarias primarias: innata y adaptativa.
La respuesta innata actúa como la primera línea de defensa, brindando protección inmediata pero no específica. Los actores clave son los macrófagos, los neutrófilos, las células dendríticas, las células asesinas naturales (NK) y los mastocitos. Los macrófagos, derivados de los monocitos, son fundamentales para eliminar patógenos y células muertas a través de la fagocitosis, al mismo tiempo que liberan citocinas proinflamatorias como las interleucinas-1 (IL-1), IL-6 y el factor de necrosis tumoral α (TNF-α) para reclutar células inmunitarias adicionales en los sitios de infección.
Por el contrario, la respuesta inmunitaria adaptativa se caracteriza por su especificidad y memoria, lo que proporciona una inmunidad duradera. Esta respuesta involucra a las células B y T. Al encontrarse con antígenos específicos, las células B se activan y se diferencian en células plasmáticas, que secretan anticuerpos, y células B de memoria, que aseguran respuestas rápidas en exposiciones posteriores.
Las células T se dividen en células T auxiliares (células T CD4+) y células T citotóxicas (células T CD8+). Las auxiliares coordinan la respuesta inmunitaria liberando citocinas que activan las células B y las T citotóxicas, al tiempo que mejoran la función de los macrófagos. Las células T citotóxicas atacan directamente y matan a las células infectadas o cancerosas al reconocer antígenos específicos presentados en las moléculas de clase I del complejo mayor de histocompatibilidad.
Los niveles elevados de hormonas del estrés, en particular de cortisol, pueden suprimir la actividad de las células inmunitarias clave y sesgar la producción de citocinas, lo que resulta en un debilitamiento de la respuesta inmunitaria. Esta alteración puede conducir a una menor producción de anticuerpos y una función deteriorada de las células T, lo que en última instancia compromete la capacidad del cuerpo para combatir infecciones y mantener la salud general.
Por otra parte, el estrés puede inducir cambios en la distribución y el comportamiento de las células inmunitarias, como una reducción de las células T circulantes y las células NK, que son vitales para reconocer y eliminar las células infectadas o cancerosas. Este cambio puede disminuir la vigilancia inmunitaria y aumentar la susceptibilidad a enfermedades infecciosas y afecciones inflamatorias crónicas.
| Respuestas fisiológicas y fisicoquímicas al estrés |
Los seres humanos reaccionan al estrés a través de mecanismos fisiológicos que involucran los sistemas simpáticos adrenomedular e hipotálamo-hipofisario-adrenal (HPA). Las reacciones de estrés prolongadas o desreguladas pueden aumentar la carga alostática y el riesgo de infecciones, enfermedades cardíacas e hipertensión.
La exposición al estrés crónico es común en el estilo de vida actual y tiene un impacto en la salud mental, además de exacerbar potencialmente enfermedades como la diabetes, la obesidad, el cáncer y las enfermedades cardiovasculares (ECV).
Por otra parte, el estrés puede ser inducido por la exposición a la contaminación. Los contaminantes regulan las respuestas al estrés al afectar los sistemas biológicos. El eje HPA del sistema endocrino regula principalmente la respuesta al estrés.
En neurobiología, los ejes alopregnanolona y HPA desempeñan papeles importantes en el trastorno depresivo mayor (TDM) y el trastorno por estrés postraumático (TEPT). La exposición a un estrés grave puede alterar estos niveles al disminuir los niveles de alopregnanolona, lo que induce TEPT y TDM.
La conducta, el metabolismo y la regulación del sistema inmunitario están muy influenciados por el eje intestino/cerebro, mediado por la microbiota intestinal, la barrera intestinal y el sistema nervioso central. Por lo tanto, en este sentido, mantener una dieta equilibrada y una actitud libre de estrés puede ser un enfoque potencialmente favorable.
El estrés suele cambiar el funcionamiento psicológico del cerebro. También, aunque las respuestas cardiovasculares al estrés atenuadas rara vez se asocian con la ECV, están vinculadas a factores de riesgo conductuales específicos para la ECV, como ciertos hábitos y la depresión.
| Vías que conectan el estrés con la función inmunitaria |
El eje HPA desempeña un papel central en la respuesta del cuerpo al estrés. Ante la exposición a un factor estresante, el hipotálamo libera la hormona liberadora de corticotrofina (CRH), que estimula la hipófisis anterior para que secrete hormona adrenocorticotrófica (ACTH). Esto impulsa a la corteza suprarrenal a producir cortisol, un glucocorticoide fundamental para modular las respuestas inmunológicas.
El cortisol tiene un doble efecto sobre la función inmunitaria. A corto plazo, mejora la actividad de las células específicas, como las NK, y promueve la producción de citocinas proinflamatorias, incluidas IL-6 y TNF-α. Sin embargo, la exposición crónica a niveles elevados de cortisol puede provocar desregulación inmunitaria e inmunosupresión.
La exposición prolongada al cortisol reduce la proliferación y la actividad de las células T, lo que disminuye la capacidad del organismo para generar respuestas inmunitarias efectivas. Este efecto inmunosupresor está bien documentado, particularmente en casos de estrés crónico. Por ejemplo, Zhang et al. (2020) hallaron que los niveles elevados de cortisol estaban relacionados con la menor activación y proliferación de las células T en los pacientes con estrés crónico, lo que pone de relieve de qué manera los glucocorticoides elevados pueden perjudicar las respuestas inmunitarias adaptativas, aumentando la vulnerabilidad a las infecciones y reduciendo la eficacia de las vacunas.
Además del eje HPA, el SNS juega un papel fundamental en la respuesta al estrés. Su activación conduce a la liberación de catecolaminas, incluidas la adrenalina y la noradrenalina, que pueden afectar directamente la función de las células inmunitarias. Pueden mejorar la actividad de las células inmunitarias innatas, como las NK y los los macrófagos, pero pueden inhibir la inmunidad adaptativa, al alterar la función de las células T y las células B.
Se ha demostrado que la exposición prolongada a catecolaminas regula negativamente la expresión de los receptores de células T CD4+ y CD8+, lo que conduce a una disminución de la activación y proliferación de las células T. Esta desregulación contribuye a una respuesta inmunitaria adaptativa debilitada con implicancias significativas para la salud.
El sistema inmunitario responde al estrés a través de diversos mecanismos que pueden producir resultados tanto beneficiosos como perjudiciales, según la duración e intensidad del factor estresante. En un estudio controlado de Barrett et al. (2021), los investigadores expusieron a ratones a factores estresantes tanto a corto plazo (agudos) como a largo plazo (crónicos).
Si bien el estrés agudo favoreció la proliferación de células T y el aumento de los marcadores inflamatorios, el estrés crónico redujo significativamente la actividad celular y la función inmunitaria general. Este hallazgo destaca la importancia de considerar la duración del estrés al evaluar la eficacia inmunitaria.
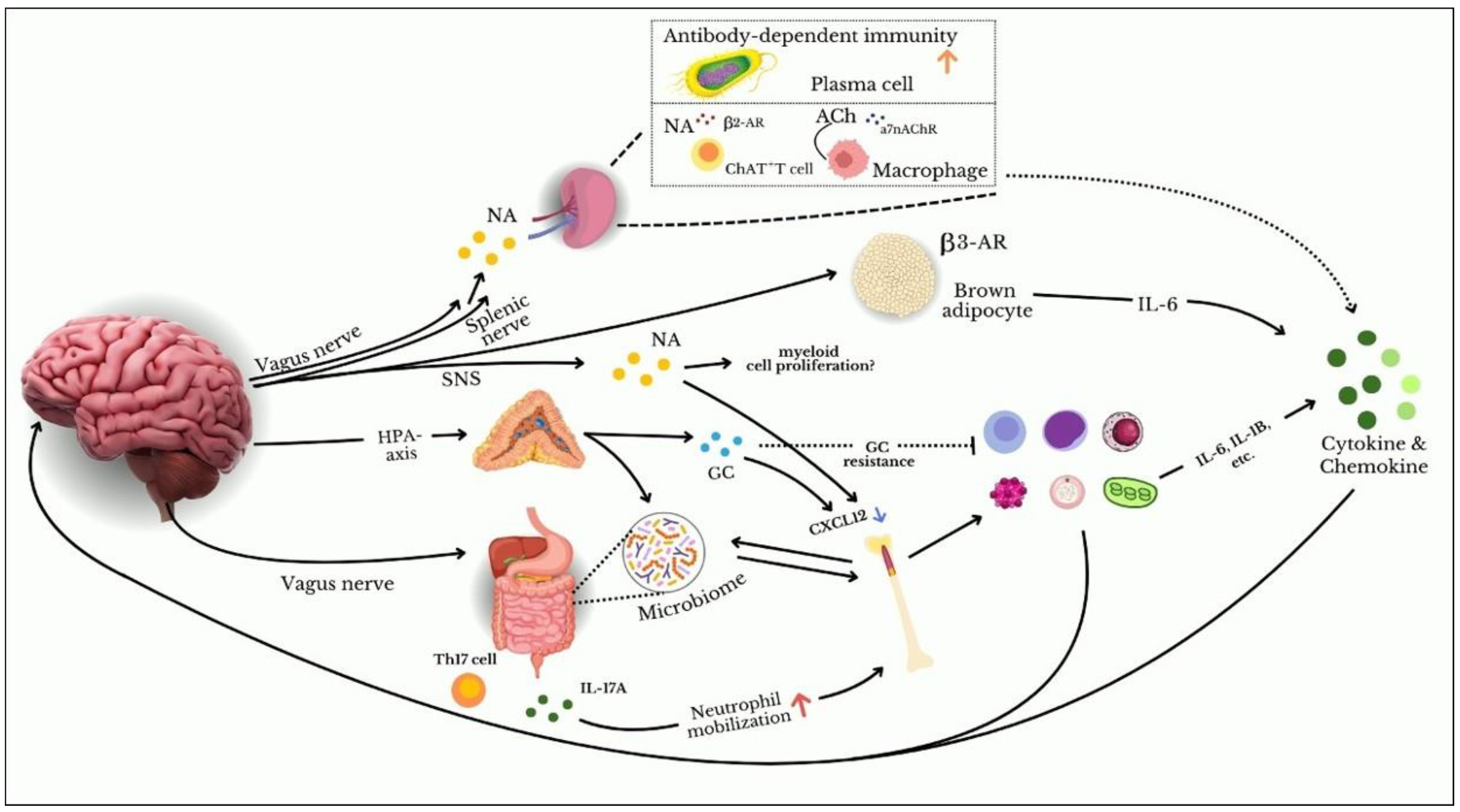
IL: interleukin; Th17: T helper lymphocyte 17; CXCL12: homeostatic chemokine ligand; β2/β3-AR: β2/β3-adrenoceptors; Ach: acetylcholine; α7nAChR: α7 nicotinic acetylcholine receptor; HPA: hypothalamic–pituitary–adrenal axis; SNS: sympathetic nervous system; NA: noradrenaline; GC: glucocorticoids. Adaptado de: Ishikawa and Furuyashiki (2022).
| Activación inmunitaria |
El estrés agudo se refiere a las respuestas inmediatas a las amenazas percibidas, activando la respuesta corporal de “lucha o huida”. Esta activación se caracteriza por un aumento rápido de las hormonas del estrés, particularmente el cortisol y la adrenalina, que pueden ser beneficiosas a corto plazo.
El estrés agudo suele conducir a una mejoría temporal de la función inmunitaria, conocida como “respuesta inmunológica inducida por estrés”, que prepara al cuerpo para responder de manera efectiva a las amenazas inmediatas. Facilita la movilización de las células inmunitarias y aumenta la producción de citocinas proinflamatorias.
Después de la exposición al estrés agudo, hay un aumento significativo de las citocinas proinflamatorias, como IL-6 y TNF-α, lo que es crucial para los procesos inflamatorios necesarios durante las lesiones físicas o las infecciones. Los estudios clínicos respaldan estos hallazgos. Por ejemplo, Cohen et al. (2007) hallaron que las personas expuestas a estrés psicológico agudo, como hablar en público, o la presión relacionada con los exámenes, exhibieron niveles aumentados de citocinas proinflamatorias circulantes y mayor actividad de las células NK.
Por otra parte, un estudio de Zhang et al. (2020) evaluó la respuesta inmunitaria de los participantes sometidos a estrés psicológico agudo, mostrando un aumento significativo de las citocinas proinflamatorias circulantes (IL-6, TNF-α) y una mayor actividad de las células NK, inmediatamente después del factor estresante. Estos hallazgos sugieren que el estrés agudo puede preparar al sistema inmunitario para responder rápidamente a amenazas potenciales.
| Estrés crónico y desregulación |
Al contrario del estrés agudo, el estrés crónico implica una exposición prolongada a factores estresantes y está asociado con efectos perjudiciales para la salud, en particular en lo que respecta a la producción de citocinas. El estrés crónico tiene un doble impacto en los niveles de citocinas, aumentando simultáneamente las proinflamatorias y antiinflamatorias.
El estrés crónico a menudo conduce al aumento de las citocinas proinflamatorias, como IL-6, TNF-α e IL-1.
La activación del eje HPA en condiciones de estrés da como resultado la liberación de glucocorticoides, principalmente cortisol. Si bien el cortisol inicialmente amortigua las respuestas inflamatorias, la exposición prolongada puede paradójicamente aumentar la producción de citocinas proinflamatorias.
Las investigaciones indican que el estrés puede inducir un estado de activación inmunitaria, en el que las células inmunitarias como los macrófagos y las células T se vuelven hiperreactivas, impulsadas por neurotransmisores relacionados con el estrés, como la noradrenalina, que puede mejorar la secreción de citocinas proinflamatorias. Por otra parte, los estudios sugieren que el estrés crónico puede alterar la expresión genética de la señalización de citocinas, lo que contribuye a un estado inflamatorio sostenido.
La elevación crónica de las citocinas proinflamatorias está relacionada con varios problemas de salud, incluidas las ECV, el síndrome metabólico y los trastornos de salud mental, como la depresión y la ansiedad. Un estudio halló que las personas que experimentaban estrés crónico exhibían niveles significativamente más elevados de IL-6, lo que se correlacionó con un aumento de los factores de riesgo de ECV. Este estrés crónico está relacionado con una mayor rigidez arterial y disfunción endotelial, ambos contribuyentes críticos del desarrollo de ECV. Por otra parte, el estado inflamatorio persistente asociado con el estrés puede exacerbar estos cambios fisiológicos, ya que la inflamación inducida por el estrés puede dañar los vasos sanguíneos y promover la aterosclerosis.
El estrés crónico también puede conducir a un aumento de los niveles de citocinas antiinflamatorias, como la IL-10 y el factor de crecimiento transformante β (TGF-β). Esta respuesta puede servir como un mecanismo compensatorio para contrarrestar los efectos de las citocinas proinflamatorias. Sin embargo, si bien los niveles elevados de citocinas antiinflamatorias pueden parecer beneficiosos, el estrés prolongado puede alterar el equilibrio entre las respuestas proinflamatorias y antiinflamatorias.
La evidencia sugiere que la elevación crónica de ambos tipos de citocinas puede conducir a una desregulación inmunitaria. Las citocinas antiinflamatorias elevadas pueden no ser suficientes para contrarrestar los efectos de las citocinas proinflamatorias, lo que resulta en una supresión inmunitaria o el desarrollo de trastornos autoinmunes.
Con el tiempo, la capacidad de respuesta de las células inmunitarias al cortisol disminuye, lo que conduce a una disminución de la expresión de los receptores de cortisol. Esta disminución da como resultado efectos antiinflamatorios reducidos del cortisol, lo que fomenta un estado de inflamación crónica. Este estrés crónico desencadena la desregulación, lo que contribuye a la aparición y brotes de varias enfermedades autoinmunes.
El estrés crónico también puede provocar una disminución de la proliferación de linfocitos T y B, lo que afecta o suprime la respuesta inmunitaria adaptativa y aumenta la susceptibilidad a las infecciones. Por ejemplo, un estudio con personas con enfermedades crónicas descubrió que quienes experimentaban estrés continuo tenían recuentos de células T y respuestas de anticuerpos significativamente menores a la vacunación contra la gripe que aquellos con niveles de estrés más bajos.
Cohen et al. (2013) también descubrieron que las personas en condiciones de alto estrés crónico eran más propensas a desarrollar infecciones de las vías respiratorias superiores. El estudio relacionó esta mayor susceptibilidad con las respuestas inmunitarias deterioradas, lo que enfatiza la relevancia clínica del tratamiento del estrés.
La relación entre el estrés crónico y la producción de citocinas es dinámica y multifacética. Las diferencias individuales, como las predisposiciones genéticas, la resiliencia psicológica y los factores ambientales, pueden influir significativamente en este equilibrio. Los estudios han demostrado que las personas con mecanismos de afrontamiento adaptativos tienden a tener un perfil de producción de citocinas más favorable.
| Modulación molecular e inmunitaria inducida por el estrés |
El estrés causa modulaciones moleculares e inmunitarias, alterando la función y la respuesta a las infecciones y enfermedades. El estrés grave puede crear un estado anérgico en el sistema inmunitario, reduciendo la inmunidad protectora y aumentando la vulnerabilidad a las infecciones. Puede activar las vías de señalización que afectan la expresión de las moléculas involucradas en la inmunidad. Esto permite que el sistema reconozca las células estresadas. El estrés también puede desencadenar la muerte celular inmunogénica, que ayuda al sistema a reconocer y eliminar a las células cancerosas.
El estrés puede alterar los mecanismos innatos al alterar el estado de activación de las células del linaje mieloide y aumentar la síntesis y liberación de proteínas inflamatorias. Estas alteraciones inducidas por el estrés afectan potencialmente la eficacia de las vacunas, las estrategias terapéuticas y la salud y el bienestar generales.
Diversos mecanismos modulan las respuestas inmunitarias a través de factores de transcripción inducidos por el estrés. Un enfoque es la activación de los factores de transcripción y enzimas sensibles a la oxidación-reducción, lo que resulta en la generación de especies reactivas de oxígeno y nitrógeno, junto con niveles alterados de antioxidantes intracelulares.
Otro enfoque es controlar el transcriptoma inmunológico a través de las vías de señalización intracelular, incluida la vía de señalización de la fosfatidilinositol 3-cinasa o la proteínacinasa B, las proteínacinasas activadas por mitógenos y la señalización de calcio.
Las respuestas inmunitarias también pueden modularse por cambios en las histonas, el ARN no codificante, los reguladores transcripcionales y la metilación del ADN. Por otra parte, la CRH es necesaria para la expresión génica inducida por el estrés en las células inmunitarias, como los esplenocitos. En conjunto, estos mecanismos ayudan a los factores de transcripción inducidos por el estrés a modular las respuestas.
Tanto el estrés agudo como el crónico se asocian con mayores niveles de citocinas proinflamatorias, incluyendo TNF-α, IL-1 ß y IL-6. Por otra parte, se ha observado una preparación neuroinmunitaria inducida por el estrés, lo que indica un historial de sensibilización del sistema inmunitario al estrés y mejores efectos proinflamatorios.
El sistema inmunitario puede activarse y desencadenarse por el estrés, lo que lleva a la liberación de citocinas proinflamatorias. Esto conduce a la exacerbación de las condiciones inflamatorias. La vía de señalización de la proteínacinasa activada por mitógeno p38 inducida por el estrés, a su vez activa factores de transcripción como la proteína de unión al elemento de respuesta a AMPc y c-Jun, que se unen a los genes estimulados por el interferón presentes en los macrófagos.
El estrés puede aumentar la actividad de unión del ADN NF-kB en las células mononucleares de sangre periférica, lo que resulta en una mayor expresión de ARNm de las citocinas proinflamatorias IL-6 e IL-1. La familia NF-kB incluye NF-kB1, NF-kB2, RELB, RELA y factores reguladores de interferón, como IRF1, IRF5, IRF7 e IRF8, que son factores de transcripción importantes involucrados con los genes de respuesta inmunitaria.
| Conclusiones |
La inmunología del estrés representa una intersección crítica entre el estrés y el sistema inmunitario, con estresores agudos y crónicos que ejercen efectos distintos. El estrés agudo activa las células inmunitarias y tiene efectos positivos a corto plazo.
Sin embargo, el estrés crónico altera significativamente la función inmunitaria, a través de mecanismos como la activación del eje pituitario adrenal y el sistema nervioso simpático, alteraciones en los perfiles de citocinas y modificaciones en la dinámica de las células inmunitarias. Estas alteraciones no solo aumentan la susceptibilidad a las infecciones y exacerban las enfermedades autoinmunes, sino que también pueden influir en la progresión de las enfermedades cardiovasculares y otros problemas de salud.
Traducción y resumen objetivo: Dra. Marta Papponetti