Introducción
La pérdida de sangre durante la resección hepática afecta la morbilidad y mortalidad perioperatorias [1]. Las transfusiones sanguíneas perioperatorias están asociadas también con una tasa más alta de recurrencia y una sobrevida más baja, después de la resección de metástasis hepáticas de origen colorrectal [2], y del carcinoma hepatocelular [3]. Los siguientes procedimientos quirúrgicos pueden disminuir considerablemente la pérdida de sangre y la necesidad de transfusión: uso de una presión venosa central (PVC) baja [4], nuevos dispositivos hemostáticos para la transección hepática [5,6], y el control del flujo vascular de entrada [5,7] y de salida [8], antes de la sección hepática.
El clampeo del pedículo hepático (maniobra de Pringle) puede producir lesiones por isquemia en el futuro remanente hepático, particularmente en los casos con enfermedad subyacente del hígado [9,10]. Esas lesiones isquémicas pueden ser prevenidas por un clampeo intermitente, de cierta extensión, de la tríada portal [11] o pre acondicionando isquemia hepática [12]. La oclusión vascular hemihepática selectiva del hígado resulta en una pérdida similar de sangre y de requerimientos de transfusión que el clampeo total del pedículo hepático [13]. Asimismo, el clampeo selectivo no ocasiona lesiones isquémicas en el remanente hepático y puede ser particularmente útil en la laparoscopía, debido a la duración más larga de la transección hepática. El clampeo del pedículo portal por períodos más largos puede producir mayores lesiones hepáticas isquémicas.
En la laparoscopía, el control vascular selectivo es facilitado por la magnificación de la imagen, permitiendo una disección muy precisa del pedículo portal, sectorial y aún de las ramas segmentarias. La presión positiva del neumoperitoneo puede jugar también un rol hemostático adicional. Por lo tanto, la resección hepática laparoscópica (RHL) con ligadura vascular del flujo de entrada, antes de la transección, puede asociarse con niveles más bajos de pérdida de sangre que la laparotomía. El objetivo de este estudio comparativo retrospectivo fue evaluar la eficacia del control vascular previo (CVP) selectivo, en pacientes sometidos a resecciones hepáticas laparoscópicas o abiertas.
Métodos
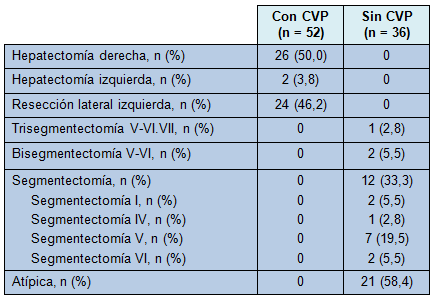
Entre 1999 y 2008, 52 pacientes fueron sometidos a RHL con CVP (hepatectomía derecha en 50%, hepatectomía izquierda en 3,8% y resección lateral izquierda en 46,2%). Las resecciones segmentarias y no anatómicas fueron realizadas sin CVP (Tabla 1). Los criterios de selección para la resección laparoscópica fueron: tumores bien separados del pedículo portal o de las venas hepáticas, un puntaje de la American Society of Anesthesiologists (ASA) menor o igual a 3, hígados no cirróticos o con cirrosis compensada, várices esofágicas menores o iguales a 1 y recuento de plaquetas mayor o igual a 80 x 109/L. Se compararon los pacientes sometidos a laparoscopía con CVP con los pacientes sometidos a cirugía abierta sin CVP, seleccionados de la base de datos de resecciones hepáticas. Los pacientes de los grupos de laparoscopía y cirugía abierta fueron emparejados por sexo, edad, puntaje ASA, tipo de resección hepática, presencia y severidad de enfermedad hepática y tamaño del tumor.
• TABLA 1: Tipos de resecciones hepáticas para los pacientes sometidos a hepatectomía laparoscópica con y sin CVP
Manejo operatorio y perioperatorio
La técnica quirúrgica, cuidados postoperatorios, recolección de datos clínicos, y análisis histológico, se realizaron como ya fuera descrito previamente [14-17]. La técnica quirúrgica de los autores es similar para las resecciones hepáticas abiertas y para la RHL, particularmente para las resecciones anatómicas del hígado. Efectivamente, en las resecciones anatómicas, los vasos portales y las venas hepáticas son controlados y seccionados antes de la transección del parénquima. En la hepatectomía derecha, la rama sectorial derecha de la vena porta y la rama derecha de la arteria hepática fueron disecadas fuera del parénquima hepático y seccionadas [18]. Para la hepatectomía izquierda, la rama portal izquierda y la rama izquierda de la arteria hepática fueron también controladas extra parenquimatosamente y seccionadas (Fig. 1). Las secciones laterales izquierdas fueron realizadas con control previo del pedículo portal separadamente para los segmentos II y III. La vena hepática correspondiente fue controlada también antes de la transección parenquimatosa.
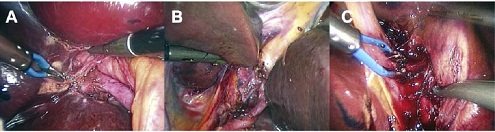
FIGURA 1: (A) Control de la rama portal derecha. (B) Control de la rama portal izquierda. (C) Control del pedículo portal para el segmento III
Para la RHL los autores emplearon una técnica enteramente laparoscópica con 5 puertos, un neumoperitoneo de 10 a 12 mmHg, un laparoscopio de 0° y un sostenedor robótico para la cámara. La transección parenquimatosa fue realizada con disección ultrasónica (Ultracision; Ethicon, Issy les Moulineaux, Francia) o con termofusión (Ligasure; Covidien, Elancourt, Francia). Se usó coagulación bipolar para tratar el sangrado menor.
Criterios del estudio
Las variables quirúrgicas evaluadas fueron la duración de la intervención, pérdida de sangre, tasa de transfusión, tasa de conversión y márgenes de la resección. Las variables postoperatorias investigadas fueron la morbilidad global y específica, mortalidad perioperatoria y duración de la estadía hospitalaria. Las complicaciones postoperatorias fueron clasificadas como específicas en relación con el hígado (esto es, descompensación cirrótica, hemorragia o colección biliar) y complicaciones generales. La gravedad de la complicación fue estratificada de acuerdo con la clasificación modificada de Clavien [19].
Análisis estadístico
El apareamiento y los análisis estadísticos fueron realizados con el programa NCSS 2007 (NCSS, LLC, Kaysville, UT). Las variables continuas fueron expresadas como medias ± desviación estándar (DE) y fueron comparadas usando la prueba U de Mann-Whitney. La prueba exacta de Fisher fue empleada para la comparación de las variables categóricas. Los valores de P < 0,05 fueron considerados estadísticamente significativos.
Resultados
Parámetros demográficos
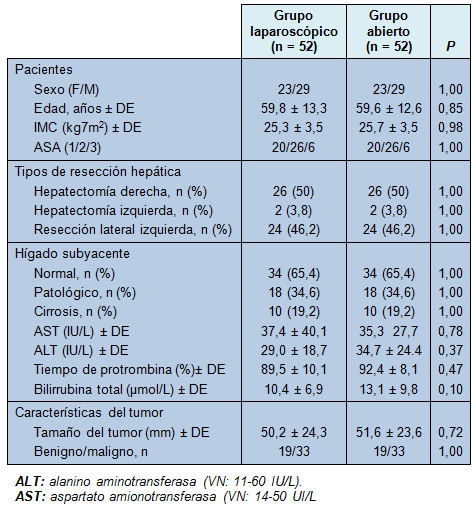
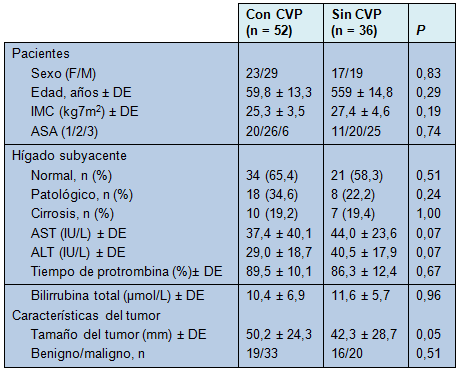
Cincuenta y dos pacientes fueron sometidos a RHL con CVP y fueron comparados en un análisis de casos apareados con 52 pacientes seleccionados retrospectivamente de la base de datos de cirugía abierta. Los dos grupos de pacientes fueron también similares en términos de índice de masa corporal (IMC), resultados de las pruebas sanguíneas hepáticas preoperatorias y tipo histológico del tumor resecado (benigno/maligno) (Tabla 2).
• TABLA 2: Características demográficas de los pacientes sometidos a hepatectomía laparoscópica y abierta con CVP y características de sus tumores e hígados
Resultados quirúrgicos
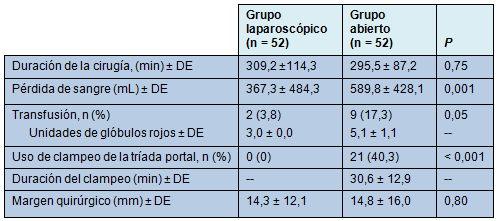
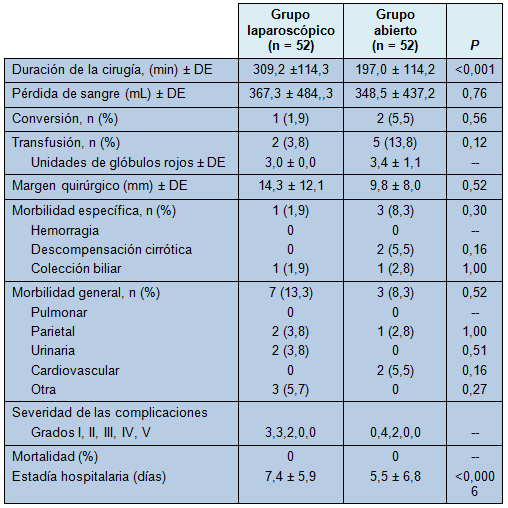
No hubo diferencia en el tiempo operatorio entre los 2 grupos (309 minutos para la laparoscopía vs 295 minutos para la laparotomía; P = 0,75; Tabla 3). La maniobra de Pringle fue usada en el 40% de los pacientes en el grupo de cirugía abierta y en ninguno de los sometidos a laparoscopía. Sin embargo, la pérdida de sangre y la tasa de transfusión fueron más bajas en el grupo de laparoscopía (367 mL vs 589 mL; P = 0,001; trasfusiones: 3,8% vs 17,3%; P = 0,05, respectivamente). No hubo diferencia en el margen quirúrgico entre los 2 grupos (P = 0,80).
• TABLA 3: Resultados quirúrgicos para los pacientes sometidos a hepatectomía laparoscópica y abierta con CVP
Resultados postoperatorios
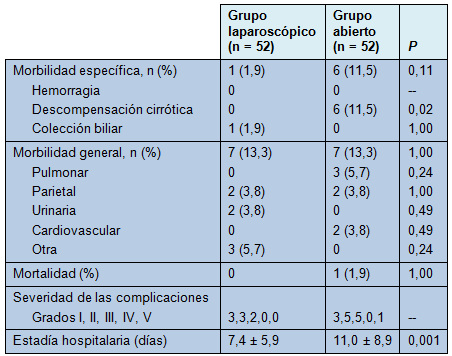
La morbilidad específica y general no difirieron significativamente entre los 2 grupos (específica: 1,9% vs 11,5% en los grupos de laparoscopía y laparotomía, respectivamente; P = 0,11; general: 13,3% vs 13,3% en los grupos de laparoscopía y laparotomía, respectivamente; P = 1,00; Tabla 4). No obstante, todos los casos de ascitis fueron observados en el grupo de cirugía abierta (11,5%), sin haberse identificado casos en el grupo de laparoscopía (P = 0,02). Un paciente cirrótico en el grupo de laparotomía falleció por insuficiencia hepática a los 40 días después de la cirugía. La estadía hospitalaria fue más prolongada en el grupo de cirugía abierta (11 vs 7,4 días; P = 0,001).
• TABLA 4: Resultados postoperatorios para los pacientes sometidos a hepatectomía laparoscópica y abierta con CVP
Comentarios
Se han descrito varios procedimientos para disminuir la pérdida de sangre y la necesidad de transfusiones perioperatorias, lo que se asocia con la morbilidad y mortalidad perioperatorias y una pobre sobrevida [1-3]. El CVP selectivo ha demostrado que disminuye eficientemente el sangrado o los requerimientos de transfusión, particularmente en pacientes con un parénquima patológico [9]. En este estudio, sus autores mostraron la factibilidad del CVP durante la RHL y la eficacia más grande de ese abordaje laparoscópico comparado con la cirugía abierta.
La cirugía laparoscópica del hígado es reconocida en la actualidad como un procedimiento seguro, con mejores resultados quirúrgicos y postoperatorios comparado con la laparotomía, para las resecciones hepáticas menores [20]. Las resecciones laparoscópicas mayores exitosas han sido reportadas recientemente por equipos de expertos en cirugía hepática y laparoscopía [16,18,21-24]. Los autores de este trabajo han mostrado previamente la eficacia del CVP durante la hepatectomía derecha laparoscópica [16]. En esta serie, el CVP durante la RHL fue posible en la mayoría de las hepatectomías anatómicas derechas e izquierdas y en las resecciones laterales izquierdas. Los autores creen también que la magnificación alcanzada con el laparoscopio permite una disección precisa de los pedículos portales, facilitando su control extra parenquimatoso. Además, la posición del laparoscopio (esto es, paralelo a la vena cava) brinda una excelente visión del espacio retrohepático y de la confluencia hepatocaval.
La pérdida de sangre y la tasa de transfusiones fueron significativamente más bajas en los pacientes sometidos a laparoscopía que en aquellos sometidos a laparotomía. Estudios comparativos previos han reportado niveles más bajos de pérdida sanguínea durante la laparoscopía pero no identificaron diferencias significativas en la tasa de transfusiones [25-31]. La mayoría de ellos involucraron resecciones no anatómicas o resecciones anatómicas sin CVP. La superioridad de los nuevos dispositivos hemostáticos para la transección del parénquima, desarrollados específicamente para la RHL sobre el método de aplastamiento convencional con un clamp, no ha sido aún demostrada [6]. Por lo tanto, los autores sugieren que durante la RHL el sangrado es esencialmente controlado por el CVP; ese efecto es reforzado por el neumoperitoneo, que puede jugar un rol hemostático adicional. Efectivamente, la presión vascular sobre el muñón hepático está relacionada con el flujo de entrada (disminuido por el CVP), el flujo de salida (disminuido por una PVC baja) y la contrapresión del neumoperitoneo. Se ha demostrado que el neumoperitoneo con presión positiva puede disminuir la pérdida hemática causada por el trauma en un modelo animal [32]. La presión intraabdominal usada por los autores en la RHL fue de alrededor de 10 a 12 mmHg y puede incrementarse a 15 mmHg en casos de sangrado más serio por el muñón hepático. El uso de un PVC baja durante la laparoscopía se asocia con un aumento teórico en el riesgo de embolia por dióxido de carbono, cuando las presiones de insuflado exceden la PVC, causando un gradiente de presión en la circulación venosa [33]. El impacto del neumoperitoneo es bien conocido y la posibilidad de efectos adversos, particularmente en pacientes con riesgo alto, ha sido descartada [34]. La embolia por dióxido de carbono ocurre frecuentemente durante la RHL [35]. En un modelo animal, se encontró que tenía efectos clínicos mínimos [36].
Dos estudios comparativos se han enfocado sobre la duración del clampeo de la tríada portal y mostraron que era más prolongado en la laparoscopía [29,31]. La maniobra de Pringle durante la RHL puede conducir a cambios cardiovasculares significativos, particularmente en pacientes con enfermedad cardíaca preexistente [37]. Asimismo, se ha demostrado recientemente, en un modelo porcino, que el clampeo de la tríada portal durante la laparoscopía, asociado con un aumento en la presión intraabdominal, puede alterar la circulación reversa por la vena hepática, induciendo a una isquemia hepática más grave que con el clampeo pedicular realizado en la laparotomía [38]. Esos hallazgos apoyan la conclusión de los autores de este trabajo de que el
CVP selectivo es más adecuado que el clampeo portal completo para la RHL.
Los autores realizaron también un segundo análisis, en el que compararon la RHL con CVP con la RHL sin CVP. Basados en su experiencia con la RHL, realizaron todas las resecciones laterales izquierdas y las RHL mayores con CVP (Tabla 1). Aunque la RHL sin CVP incluyó sólo a las resecciones segmentarias y a las no anatómicas, no se observó una diferencia estadísticamente significativa en la pérdida de sangre o en la tasa de transfusiones entre los 2 grupos. Eso puede explicarse por el hecho de que en las secciones laterales izquierdas y en las hepatectomías derecha e izquierda, la transección del hígado a través de un abordaje anterior-posterior, facilitando la división a través del control directo de los distintos vasos, que son encontrados siempre en un plano horizontal. En las resecciones segmentarias y no anatómicas, la división del hígado se realiza en diferentes planos, haciendo más difícil exponer el muñón hepático. Los tumores anteriores pequeños tratados con resecciones segmentarias y no anatómicas pueden parecer los más adecuados para la RHL, pero en realidad pueden ser los más demandantes. En la visión de los autores de este trabajo, las resecciones anatómicas formales, típicamente las resecciones laterales izquierdas, son los mejores procedimientos para cirujanos no experimentados que desean comenzar a realizar RHL. Además, no hallaron diferencia entre los 2 grupos en términos de margen quirúrgico a pesar del hecho de que los tumores más grandes fueron incluidos en el grupo con CVP (Tabla 5). La cirugía fue más prolongada en el grupo con CVP, debido parcialmente al paso adicional de disección vascular, pero eso refleja también la inclusión en este grupo de todas las resecciones mayores. Asimismo, la tasa de conversión y los resultados postoperatorios (excepto la estadía hospitalaria) no difirieron significativamente entre los 2 grupos (Tabla 6).
• TABLA 5: Características demográficas de los pacientes sometidos a hepatectomía laparoscópica con y sin CVP y características de sus tumores e hígados
• TABLA 6: Resultados quirúrgicos y postoperatorios de los pacientes sometidos a hepatectomía laparoscópica con y sin CVP
La magnificación de la laparoscopía permite una disección muy precisa de los pedículos portales y de las venas hepáticas y hacen factible y seguro el CVP. Los datos de este trabajo sugieren que el CVP es más efectivo en la RHL que en la cirugía abierta. Esos resultados alientan a los cirujanos de hígado experimentados a expandir el uso de la laparoscopía en las resecciones hepáticas anatómicas, aún en las hepatectomías mayores.
♦ Comentario y resumen objetivo: Dr. Rodolfo D. Altrudi