Introducción
La terapia endoscópica se ha convertido recientemente en un tratamiento aceptado de primera línea para la displasia de alto grado (DAG) y el cáncer intramucoso (CIM) [1]. Dos ensayos controlados randomizados [2,3] y múltiples series de casos [4-19] han demostrado baja morbilidad, tasas bajas de progresión del cáncer esofágico y tasas altas de erradicación exitosa de la enfermedad, mediante ablación por radiofrecuencia (ARF) o resección mucosa endoscópica (RME) o ambas. No obstante, se conoce poco sobre los resultados en los pacientes en quienes persisten las células displásicas, aquellos en los que hay recidiva de la displasia o aquellos en donde hay progresión de la displasia al cáncer. En aquellos pacientes en los que fracasa la endoterapia, existe la preocupación de que con el tratamiento persistente con esas modalidades, una enfermedad localmente curable pueda progresar a un cáncer invasor.
En esos estudios iniciales, el tratamiento exitoso con la endoterapia se había basado en estrictos criterios de entrada [3,7]. Sin embargo, a medida que más endoscopistas realizan endoterapia y tratan pacientes que no reúnen esos criterios estrictos de entrada, se requiere una investigación adicional para determinar qué pacientes pueden tener un riesgo más alto de fracaso del tratamiento y revisar los resultados del mismo. Los autores de este trabajo identificaron un grupo de pacientes con DAG y CIM en los que la endoterapia fracasó y los compararon con otros pacientes que habían tenido una erradicación endoscópica exitosa, para tratar de identificar los factores que pueden predecir a aquellos pacientes en los que la endoterapia fracasará y para recoger información sobre los resultados de los tratamientos de salvataje después del intento de endoterapia.
Pacientes y métodos
Se realizó una revisión retrospectiva de los pacientes que fueron sometidos a ARF o RME (o ambas), para DAG o CIM (o ambos), en un único centro de referencia, desde 2007 hasta 2012. Los pacientes fueron identificados de una base de datos mantenida prospectivamente e incluidos en este estudio si tenían muestras de biopsia con DAG o CIM o ambos. Para su inclusión, se requirió que los pacientes hubieran sido sometidos a tratamiento inicial con RME con intención curativa o ARF con el sistema HALO (Covidien Entherapy/BarrX, Sunnyvale, CA), o ambos. Los pacientes fueron excluidos si habían tenido una RME para estadificación seguida de esofagectomía, si habían recibido terapia fotodinámica, o si no tenían DAG/CIM en la revisión centralizada de los resultados de sus biopsias, la que fue realizada por patólogos gastrointestinales experimentados con la metaplasia de Barrett.
Las biopsias sistemáticas fueron realizadas después de identificarse una DAG o CIM, para confirmar el diagnóstico y para investigar enfermedad sincrónica. La ecografía endoscópica fue usada en los pacientes con metaplasia de Barrett nodular o si el CIM fue identificado antes de cualquier tratamiento y, nuevamente, antes de realizarse la esofagectomía. La RME fue efectuada si había una lesión visible o un área pequeña de metaplasia displásica de Barrett potencialmente resecable, con el objetivo de remover toda mucosa visible elevada o nodular. La RME fue efectuada con una cápsula o con técnica de mucosectomia multibanda. La ARF fue realizada después de lavar la mucosa con 60 a 100 mL de N-acetil-cisteína diluida, ya sea con un catéter balón de 360º o con una cápsula montada en un endoscopio de 90º, utilizando el protocolo estándar de 12 J a 40 W por ablación, siendo cada área sometida a 2 ablaciones seguidas de remoción de coágulos y luego otras 2 ablaciones. Las sesiones de endoterapia fueron efectuadas con intervalos de 8 semanas, o cuando se alcanzaba la cicatrización de la mucosa, para minimizar el riesgo de estenosis. Se permitieron sesiones múltiples de endoterapia (RME o ARF o ambas). La ablación fue continuada con el objetivo de la erradicación completa de la displasia, neoplasia y metaplasia no displásica de Barrett, pero no se requirió la erradicación completa de la metaplasia, en esta serie, para considerar al tratamiento como exitoso. La ablación por coagulación con plasma de Argón fue permitida sólo después de un tratamiento inicial con ARF.
La decisión de detener la endoterapia fue tomada por los endoscopistas tratantes (DBS, BEL y AGB) después de fracasar una repetición de RME, cuando había una obvia progresión multifocal del cáncer, o cuando el paciente y el endoscopista juzgaron cambiar el tratamiento. El fracaso del tratamiento en este estudio fue definido como el hallazgo patológico de enfermedad displásica/neoplásica persistente (por ej., falla en erradicar la enfermedad), la presunción de progresión de enfermedad basada en los resultados de las biopsias realizadas usando el protocolo de Seatle [20], o enfermedad recurrente después de un intervalo de sobrevida libre de enfermedad entre 2 endoscopías sucesivas con biopsias. El éxito del tratamiento se definió por la erradicación del CIM y la DAG en un mínimo de 2 endoscopías sucesivas con biopsias. Todas las muestras de biopsias, incluyendo aquellas de los pacientes derivados al centro asistencial, fueron revisadas por patólogos gastrointestinales experimentados, del centro donde se desempeñan los autores del trabajo.
Las pruebas utilizadas para las comparaciones estadísticas fueron la de t para las variables continuas, 2 de Pearson con corrección de Yates para variables discretas y exacta de Fisher para variables discretas con frecuencias celulares menores que 5. Todos los valores de P fueron de 2 colas y no se hicieron ajustes para comparaciones múltiples. Un valor de P menor que 0,05 fue considerado estadísticamente significativo. Todos los análisis estadísticos fueron realizados utilizando el programa R (www.r-project.org). El Institutional Review Board of Swedish Medical Center aprobó este estudio y dispensó el requerimiento del consentimiento informado, por la naturaleza retrospectiva del mismo.
Resultados
Se identificaron 41 pacientes que habían sido sometidos a endoterapia. Tres fueron excluidos durante la revisión anatomopatológica porque la DAG presumida fue reclasificada como displasia de bajo gado (DBG) por 2 patólogos; por lo tanto, 38 pacientes fueron incluidos en este análisis. Veintiocho pacientes (74%) tuvieron una erradicación exitosa de la displasia y cáncer, sin recidivas. La endoterapia fracasó en 10 pacientes (26%): 1 fracaso fue causado por progresión desde CIM a CIM multifocal, 6 resultaron por progresión desde DAG a CIM y 3 fueron debidos a recidiva del CIM. Un paciente tuvo recidiva a los 12 meses con CIM en la unión neoescamocolumnar y fue sometido a esofagectomía; el CIM se desarrolló en un paciente a los 13 meses. por erupción a través de la línea neoescamosa y fue sometido a una RME de salvataje y 1 CIM se desarrolló en un paciente a los 20 meses en una sección de metaplasia de Barrett no displásica menor de 1 cm y el paciente fue sometido a esofagectomía.
Los datos demográficos fueron similares entre los 2 grupos, excepto que el grupo con éxito en el tratamiento tuvo un índice de masa corporal (IMC) mayor (Tabla 1). En el grupo con fracaso del tratamiento, hubo significativamente más pacientes con metaplasia de Barrett nodular o ulcerada, DAG multifocal y DAG en la endoscopía inicial, pero no hubo diferencia en la longitud de la metaplasia de Barrett entre los 2 grupos (Tabla 2).
• TABLA 1: Características de los pacientes
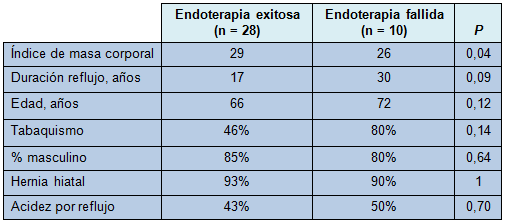
• TABLA 2: Hallazgos endoscópicos
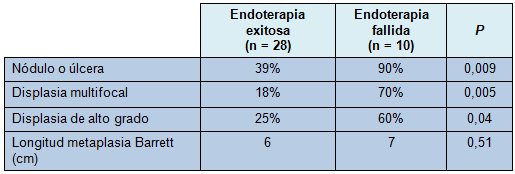
La metaplasia de Barrett no displásica persistente, fue significativamente más común en la rama de falla del tratamiento, a pesar del hecho de que esos pacientes fueron sometidos significativamente a más sesiones de endoterapia. Similarmente, los pacientes en los que fracasó la endoterapia, fueron tratados por un tiempo más largo, aunque eso no alcanzó una significación estadística. Se desarrolló 1 estenosis en cada grupo; no hubo otra morbilidad de la endoterapia (Tabla 3).
• TABLA 3: Morbilidad de la endoterapia
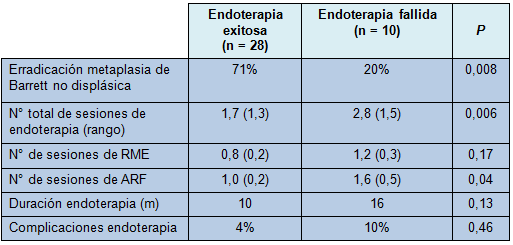
En el grupo con fracaso del tratamiento se encontró que tenían una DAG o un CIM en la endoscopía inicial, en el 60% de los casos. Durante la endoterapia, toda enfermedad en el grupo de fracaso del tratamiento, había progresado a CIM, lo que fue confirmado en el examen anatomopatológico final en todos excepto 1 paciente. Ese paciente particular tenía un CIM en los resultados de la biopsia justo antes de la esofagectomía, pero sólo se halló una DBG en la pieza operatoria. En contraste, la enfermedad en el grupo con éxito del tratamiento mejoró desde DAG y CIM a epitelio neoescamoso y metaplasia no displásica de Barrett (Tabla 4).
• TABLA 4: Condición anatomopatológica en diferentes estadios de la endoterapia
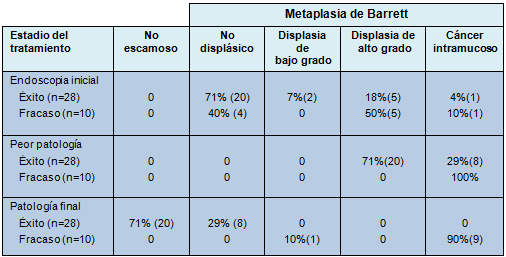
Siete de los 10 pacientes en quienes la endoterapia fracasó, fueron sometidos a esofagectomía, 1 eligió quimio-radioterapia definitiva, 1 fue médicamente no apto para la cirugía y se lo sometió a una nueva ARF y 1 tuvo una resección endoscópica de un CIM recidivado. El examen anatomopatológico final en los pacientes sometidos a esofagectomía fue CIM en 6 pacientes y DBG en 1 paciente; todos los casos fueron N0. Los pacientes tratados con esofagectomía estuvieron libres de enfermedad por una media de 25 meses postoperatoriamente. Hubo 1 muerte (14%) causada por insuficiencia respiratoria después de esofagectomía. Dos pacientes (29%) tuvieron morbilidad después de la esofagectomía: 1 tuvo una fístula anastomótica y 1 tuvo insuficiencia respiratoria postoperatoria. Excepto por la muerte perioperatoria, los restantes 9 pacientes en los que fracasó el tratamiento están vivos, con una media de 41 meses, después del diagnóstico inicial con displasia. Los pacientes que fueron sometidos a esofagectomía están todos libres de metaplasia de Barrett y no ha habido cáncer esofágico recidivado o metastásico. Comparativamente, el 71% del grupo con tratamiento exitoso no tuvo evidencias de esófago de Barrett. Diez de esos pacientes han sido sometidos a operaciones anti-reflujo laparoscópicas y 3 están siendo preparados actualmente para reparación laparoscópica.
Comentarios
El surgimiento de la RME y de la ARF en el tratamiento de la metaplasia de Barrett con DAG o CIM, ha llevado a un cambio paradigmático en el manejo de la neoplasia esofágica temprana. No obstante, a pesar del éxito reportado de esas terapias, la endoterapia fracasará en un pequeño porcentaje de pacientes, a causa de la persistencia, progresión desde displasia a cáncer invasor, o recidiva de la displasia o del cáncer, durante el seguimiento alejado. Los autores de este trabajo identificaron varios factores asociados con el fracaso de la endoterapia: DAG en el resultado de la biopsia inicial, DAG multifocal, metaplasia de Barrett nodular o ulcerada y falla para erradicar completamente una metaplasia de Barrett no displásica.
La presencia de DAG multifocal fue también identificada como un factor de riesgo para la recidiva de la displasia en un estudio previo de DAG o CIM recurrentes después de la endoterapia. A diferencia de este estudio, en donde se vieron segmentos largos de metaplasia de Barrett en ambos grupos, ese estudio tuvo una proporción significativa de segmentos más cortos de metaplasia de Barrett en el grupo en el que la enfermedad no recidivó. En ese estudio no se usó la ARF y eso puede ser el porqué la resección fragmentaria y la falla para erradicar el epitelio no displásico de Barrett fueron también factores independientes de riesgo asociados con la recidiva [9]. En otro estudio, la metaplasia de Barrett de segmento largo y la falla para erradicar la metaplasia de Barrett no displásica, fueron nuevamente identificadas como factores de riesgo para la recidiva de la DAG/CIM después de la terapia de ablación ± RME [11]. Ese estudio identificó también a la mayor edad y al tabaquismo como factores de riesgo para el fracaso. Los autores del presente estudio asociaron también esos factores con el fracaso, pero no fueron estadísticamente significativos (Tabla 1). Ambos estudios usaron terapia fotodinámica como modalidad de ablación en lugar de ARF, por lo que su tasa de recidiva puede ser más alta, a raíz del uso de una técnica de ablación con una tasa más baja de respuesta completa [21].
Se ha demostrado que tanto la presencia de DAG nodular como multifocal se asocia con una tasa aumentada de adenocarcinoma oculto [22]. La preponderancia de la DAG en los resultados de la biopsia inicial, la metaplasia de Barrett nodular o ulcerada y la DAG multifocal en el grupo con fracaso del tratamiento, reflejan probablemente a pacientes con una enfermedad más avanzada o más agresiva. En contraste, en el grupo con tratamiento exitoso, muchos pacientes que presentaban una metaplasia de Barrett no displásica desarrollaron luego una DAG, mientras eran sometidos a endoscopías de vigilancia. La falla para erradicar la metaplasia de Barrett no displásica es un factor de riesgo para el fracaso de la endoterapia, que puede deberse a que la metaplasia residual de Barrett sigue siendo un sitio potencial para el desarrollo de displasia, porque hay daño epitelial por el reflujo continuo o a causa de otro problema subyacente que impide que esos pacientes formen epitelio neoescamoso.
Continuar con la endoterapia a pesar de la presencia de metaplasia nodular de Barrett y DAG multifocal, es una extensión del criterio original de tratamiento con la endoterapia. En los primeros ensayos trascendentes, los criterios de entrada fueron muy estrictos. Ell y col. [7], investigaron 667 casos antes de realizar 100 resecciones endoscópicas, para lograr una sobrevida a 5 años del 98%.
Similarmente, el ensayo AIM II [3], comparando la ARF con un control simulado, incluyó sólo a pacientes con metaplasia no nodular de Barrett, displasia (de bajo y alto grado) y segmentos de metaplasia de Barrett de menos de 8 cm de longitud. Aun cuando el 90% de de los tratamientos fracasados en la presente serie hubieran sido excluidos del ensayo AIM II, el 68% de los pacientes en el grupo de tratamiento exitoso también habría estado excluido del AIM II, aunque tuvieron una erradicación exitosa de su DAG/CIM y preservación de su esófago funcional. Por esa razón, los autores de este trabajo le ofrecieron a los pacientes con riesgo alto de fracaso de la endoterapia, un intento de la misma. Aconsejaron a los pacientes y establecieron las expectativas sobre el éxito de la endoterapia, porque embarcarse en la endoterapia a menudo resulta en múltiples endoscopías. Dado que no existen guías aceptadas sobre cuando abortar una endoterapia, los autores recomendaron usualmente la esofagectomía, si existía enfermedad persistente o los resultados de la biopsia sugerían progresión después de 3 sesiones de endoterapia o 12 meses de tratamiento, basado en los hallazgos consignados en la Tabla 3.
Se alcanzó una tasa similar de erradicación de DAG y de CIM (74%) en esta serie, comparado con el 81% en el ensayo AIM II sólo para DAG. A los pacientes que tuvieron un tratamiento exitoso, se los alentó para que consideraran una cirugía laparoscópica antirreflujo después de un intervalo de 12 meses libre de enfermedad, para controlar mejor su reflujo. También recomendaron vigilancia endoscópica continua a intervalos similares a los recomendados por Titi y col. [23]. Los datos de este estudio, así como los de otros autores [2,23,24] apoyan la vigilancia continua, porque se identificaron 3 pacientes que habían tenido erradicación de la metaplasia comprobada por biopsia (con intervalos libres de enfermedad desde12 meses hasta 20 meses), que presentaron recurrencia de la displasia o del cáncer. Esas recidivas fueron identificadas en la unión neoescamocolumnar y en nivel subescamoso, con erupción a través del revestimiento neoescamoso. Se han reportado otros casos de DAG/CIM subescamosos [2,23,24] y la presencia de células displásicas enterradas después de la ablación es preocupante.
Existe una variedad de opciones de tratamiento para los pacientes con enfermedad persistente, progresiva o recurrente, incluyendo esofagectomía, endoterapia repetida y quimio-radioterapia definitiva. En este estudio, la mayoría de los pacientes fue sometida a esofagectomía después de la estadificación con ecografía endoscópica y tomografía por emisión de positrones/tomografía computada. En los pacientes con reestadificación negativa y CIM en la RME, se les ofreció una esofagectomía transhiatal con preservación vagal, para tomar ventaja de la función de contracción del estómago superior [25]. Cuando había preocupación por un cáncer más avanzado, se efectuó una esofagectomía en bloque. Se podría criticar a los autores de este trabajo por usar una esofagectomía más funcional sobre una con más principios oncológicos; no obstante, los autores consideran que con una re-estadificación cuidadosa y un cáncer limitado a la mucosa, en los resultados de la biopsia endoscópica, había una baja probabilidad de diseminación ganglionar. Los autores de este trabajo no tienen datos suficientes para comentar sobre los pacientes en los que la endoterapia fracasó y que fueron tratados con repetición de la terapia endoscópica o con quimio-radioterapia definitiva.
Desafortunadamente, prácticamente no se han reportado datos clínicos del seguimiento alejado, en los pacientes sometidos a esofagectomía después de endoterapia. De 44 pacientes que fueron identificados en la literatura, había información del seguimiento alejado en sólo 2 pacientes: 1 falleció por cáncer esofágico metastásico [5] y uno estaba libre de enfermedad a los 19 meses [12]. La serie presente demuestra buenos resultados clínicos y patológicos de la esofagectomía después de la endoterapia fracasada. Sin embargo, la morbilidad y mortalidad en ese subconjunto muy pequeño de pacientes sometidos a esofagectomía en el centro en donde se desempeñan los autores, son más altas que lo reportado previamente para la resección primaria de DAG y CIM sin endoterapia [10,15,17,19,25-29]. Eso puede resultar de la selección de pacientes para la endoterapia: los autores efectuaron endoterapia más agresivamente, para evitar la esofagectomía en pacientes con comorbilidades médicas de alto riesgo. Alternativamente, la endoterapia pudo haber alterado los resultados de la esofagectomía; se encontró más fibrosis mediastinal y planos obliterados en los pacientes con segmentos más largos de metaplasia de Barrett sometidos a ablación serial, tanto para los pacientes que fueron sometidos a esofagectomía después de endoterapia fracasada, como en pacientes que fueron sometidos a cirugía laparoscópica anti-reflujo después de una endoterapia exitosa.
Existen varias limitaciones para esta serie. Primero, se trata de un estudio retrospectivo y las asociaciones identificadas por sus autores no pueden ser vistas como factores causativos para el fracaso del tratamiento. Segundo, la tasa de fracaso (24%) es más alta que la de otras series de endoterapia reportadas. Eso puede deberse a la falta de un denominador exacto, porque se trata de un centro terciario de referencia y no capturó a todos los pacientes sometidos a endoterapia en su población, o porque los endoscopistas han extendido la endoterapia a pacientes que podrían no haber sido elegibles para su inclusión en los primeros estudios. Tercero, lo que los autores llaman progresión de la enfermedad durante la endoterapia, puede ser causada por error de muestreo, porque el cáncer esofágico puede ser encontrado en el examen anatomopatológico final en el 11% al 65% de las esofagectomías realizadas por DAG [26-30].
En conclusión, aún cuando la endoterapia alcanza tasas excelentes de erradicación de la DAG y del CIM, un número pequeño de pacientes tendrán una displasia o neoplasia persistente, progresiva o recurrente. La DAG en la endoscopía inicial, displasia multifocal, anomalías mucosas (úlceras o nódulos) y la falla en erradicar la metaplasia de Barrett no displásica, se asociaron con el fracaso de la endoterapia en esta serie. Si se intenta la endoterapia en pacientes con esas características, deben ser aconsejados de manera multidisciplinaria sobre el potencial de fracaso. Se debería considerar la esofagectomía si hay una neoplasia persistente, progresiva o recurrente, después de más de 1 año de tratamiento o más de 3 sesiones. La vigilancia endoscópica continua es obligatoria después de una endoterapia exitosa, debido al riesgo de enfermedad recidivada.
♦ Comentario y resumen objetivo: Dr. Rodolfo D. Altrudi