Introducción
EN 2001, la American College of Cardiology Foundation (ACCF)/American Heart Association (AHA) modificó la clasificación de la insuficiencia cardíaca (IC) para incluir también a los pacientes con alto riesgo de sufrir la enfermedad (etapa A; figura) pero aún no tienen alteraciones cardíacas estructurales ni evidencia clínica de IC. En 2010, Ramani et al analizaron el diagnóstico y el tratamiento actuales de la IC.
Desde entonces se ampliaron las indicaciones para el tratamiento farmacológico y con dispositivos, se produjeron importantes progresos en el apoyo circulatorio mecánico (ACM) y nuevos estudios clínicos para mejorar la asistencia de los pacientes con IC. Este artículo proporcionará una actualización exhaustiva sobre las estrategias diagnósticas y terapéuticas para la IC según su etapa (de A a D), centrándose sobre las nuevas recomendaciones y los resultados de investigaciones que pueden afectar la práctica médica.
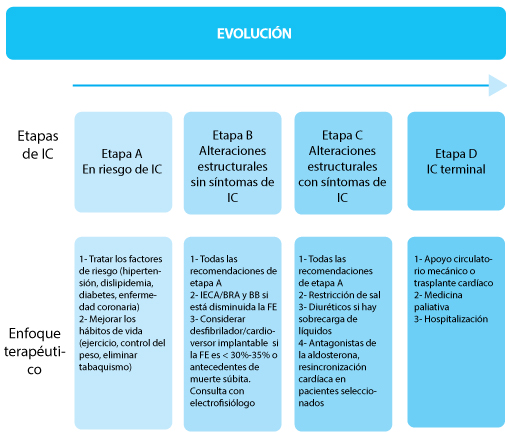
Figura. Etapas de la insuficiencia cardíaca (IC) y enfoques terapéuticos. IECA: inhibidor de la enzima convertidora de la angiotensina; BRA: bloqueante del receptor de angiotensina; BB: beta bloqueante; FE: fracción de eyección. Elaborado sobre el contenido del artículo de Dunlay et al.
| Abreviaturas y acrónimos ACCF AHA: American College of Cardiology Foundation/ American Heart Association ACM: apoyo circulatorio mecánico DAVI: dispositivo de asistencia ventricular izquierda FE: fracción de eyección IC: insuficiencia cardíaca ICAD: insuficiencia cardíaca aguda descompensada ICFEc: insuficiencia cardíaca con fracción de eyección conservada ICFEr: insuficiencia cardíaca con fracción de eyección reducida MCD: miocardiopatía dilatada NYHA: New York Heart Association SU: servicio de urgencias TRC: tratamiento de resincronización cardíaca |
IC en etapa A: Pacientes en riesgo
La etapa A de la IC comprende a los pacientes que aún no padecen IC ni alteraciones cardíacas estructurales, pero están en riesgo debido a enfermedad coronaria, diabetes, hipertensión u otros trastornos.
Pronóstico del riesgo de sufrir IC
Aunque sólo los pacientes en etapa C y D reunirían los criterios para IC, el interés por identificar a los pacientes en riesgo de IC (etapa A) hizo surgir varias puntuaciones de riesgo para IC. A partir del estudio Health ABC se creó una puntuación sencilla, basada sobre factores pronósticos independientes de IC (edad, enfermedad coronaria, presión arterial sistólica, tabaquismo, frecuencia cardíaca, glucemia en ayunas, creatininemia, albúmina).
Otro modelo para pronosticar IC validado en las cohortes del estudio ARIC (Atherosclerosis Risk in Communities) incluyó muchas de las mismas variables, así como también raza, sexo, diabetes e índice de masa corporal. Los investigadores hallaron que ambos modelos tenían capacidad pronóstico similar y eran más exactos si se agregaba el péptido natriurético tipo B N-terminal. Ambos modelos de riesgo serían aceptables para emplear en la práctica.
Pruebas genéticas en pacientes con presunta miocardiopatía familiar
El 20%-35% de los pacientes con miocardiopatía dilatada (MCD) pueden padecer miocardiopatía familiar (2 o más familiares cercanos con MCD). Ante un paciente con diagnóstico de MCD se deben obtener todos sus antecedentes familiares. Si los mismos sugieren miocardiopatía familiar es necesario efectuar pruebas genéticas y derivar para consejería genética. Las mutaciones patológicas se identifican sólo en el 30% - 35% de los casos familiares, de modo que los resultados negativos no descartan la posibilidad de una MCD. En los familiares de primer grado no afectados de pacientes con DCM familiar se debe efectuar rastreo con ecocardiografía cada 3 - 5 años.
Tratamiento para corregir los factores de riesgo modificables
En los pacientes identificados como de alto riesgo de IC se deben tratar los factores de riesgo modificables, como la hipertensión, la diabetes, la hiperlipidemia y la obesidad. El tratamiento de la hipertensión puede reducir el riesgo de IC en más del 50% y se debe basar sobre las recomendaciones publicadas, aunque un metanálisis sugirió que los diuréticos, los inhibidores de la enzima convertidora de angiotensina (IECA) y los bloqueantes del receptor de angiotensina son los más eficaces para disminuir el riesgo de IC.
IC en etapa B: Alteraciones cardíacas estructurales, pero sin síntomas clínicos de IC
La IC en etapa B incluye a pacientes con infarto de miocardio previo, remodelado ventricular izquierdo con hipertrofia del ventrículo izquierdo, disminución de la fracción de eyección (FE) y valvulopatía asintomática, que nunca tuvieron síntomas de IC. Se estima que el número de pacientes con IC en etapa B es de 3 a 4 mayor veces que el número de pacientes en etapa C y D asociados. La prevalencia de reducción asintomática de la FE es del 3% - 6% y aumenta con la edad. La disfunción diastólica asintomática es más frecuente, con prevalencia estimada de hasta el 27%.
Los pacientes con IC en etapa B tienen alto riesgo de padecer IC sintomática (etapa C), pero hay estrategias para disminuir ese riesgo. En general, en los pacientes en etapa B se deben emplear todos los tratamientos para la IC en etapa A. Otros tratamientos recomendados se indican en la figura.
La quimioterapia puede causar efectos cardíacos adversos, en especial las antraciclinas (doxorubicina, daunorubicina, epirubicina, idarubicina) y la antraquinona mitoxantrona, con incidencia de hasta el 26%. El riesgo de efectos tóxicos cardíacos aumenta con dosis acumuladas más altas y mayor edad. El empleo de bolos en lugar de infusiones continuas, doxorubicina liposomal vs noliposomal, empleo simultáneo de quelantes del hierro y administración de epirubicina o mitoxantrona (fármacos con menor riesgo de efectos cardíacos) vs doxorubicina pueden contribuir a disminuir el riesgo.
En los pacientes tratados con estos fármacos se debe evaluar la FE al inicio y después periódicamente, con suspensión de la quimioterapia si la FE disminuye en un 10% y es <50%. Todos los pacientes con disminución de la FE deben recibir IECA y β bloqueantes, igual que otros pacientes con IC en etapa B. Otros quimioterápicos que pueden causar IC son la ciclofosfamida, la ifosfamida, el trastuzumab y otros inhibidores monoclonales de la tirosina cinasa basados sobre anticuerpos.
IC en etapa C: Alteraciones cardíacas estructurales y sintomas de IC
Cuando los pacientes tienen signos y síntomas de IC se los clasifica como IC en etapa C, aunque más adelante se transformen en asintomáticos.
La ACCF/AHA publicó recomendaciones generales para el tratamiento de los pacientes con IC. Esta sección se centrará en temas importantes de investigaciones recientes sobre la IC en etapa C.
Biomarcadores para estimar el pronóstico en pacientes con IC
Aunque los biomarcadores se emplean más para diagnosticar IC, también pueden contribuir a estimar el pronóstico en pacientes con IC en etapa C y D. Los péptidos natriuréticos, especialmente el péptido natriurético tipo B o su fragmento amino-terminal (péptido natriurético tipo B N-terminal), que se liberan en respuesta a la distensión miocárdica y las troponinas, liberadas en respuesta a la lesión miocítica, son los biomarcadores más empleados para el pronóstico en la IC.
Un biomarcador surgido recientemente, el ST2, miembro de la familia de receptores de la interleucina 1, pronostica la mortalidad en la IC y puede ayudar a identificar pacientes con IC que se beneficiarían con el ajuste de la dosis de β bloqueantes. La cistatina C es un marcador de lesión renal aguda durante la hospitalización por IC y su aumento de más de 0,3 mg/l en las primeras 48 horas se asocia con mayor duración de la hospitalización y cuatro veces más mortalidad intrahospitalaria.
El valor clínico del tratamiento de la IC orientado por medición serial de los biomarcadores es polémico. El estudio en marcha GUIDE-IT puede aclarar este tema, ya que investiga la eficacia de una estrategia terapéutica orientada por biomarcadores en relación con la atención habitual en pacientes de alto riesgo con disfunción sistólica del ventrículo izquierdo.
Actualización sobre el tratamiento prolongado de pacientes con IC en etapa C
IC con FE conservada. La mitad de los pacientes con IC tienen la FE conservada (ICFEc), lo que habitualmente significa una FE > 40% - 50%. Otras enfermedades asociadas, como anemia, hipertensión y fibrilación auricular, son más frecuentes en pacientes con ICFEc que en los que sufren IC con FE reducida (ICFEr). Al igual que los pacientes con ICFEr, los pacientes con ICFEc tienen más riesgo de muerte (mortalidad a 5 años 50% en ambos grupos). Aún no hay fármacos eficaces para la ICFEc.
Hubo grandes discusiones acerca de la utilidad de los antagonistas del sistema renina-angiotensina para la ICFEc, y los resultados de los diversos estudios son contradictorios. También surgió interés en el empleo de los inhibidores de la fosfodiesterasa 5 para pacientes con ICFEc. Sin embargo, el estudio aleatorizado controlado RELAX no halló cambios en la capacidad de ejercicio o el estado clínico tras 24 semanas de tratamiento con sildenafil en relación con placebo.
Tampoco se mostraron resultados favorables sobre la capacidad de ejercicio en estudios con eplerenona, antagonista de la aldosterona (estudio RAAM-PEF), aunque sí sobre la función diastólica. El estudio TOPCAT no halló reducción del riesgo combinado de mortalidad cardiovascular, paro cardíaco fallido u hospitalización en pacientes con ICFEc tratados con espironolactona en relación con placebo. En la actualidad no hay evidencia suficiente para recomendar el tratamiento sistemático con antagonistas de la aldosterona en pacientes con ICFEc.
Evidencia creciente sugiere que la activación del sistema nervioso simpático es importante en la fisiopatología de la ICFEc. La desnervación renal es un procedimiento que se efectúa a través de un catéter transcutáneo para interrumpir los nervios simpáticos renales. Los primeros estudios en pacientes hipertensos determinaron que es segura y eficaz. El estudio DIASTOLE está investigando si la denervación renal podría ser una opción terapéutica eficaz para pacientes con ICFEc.
Los pacientes con ICFEc deben seguir con tratamiento intensivo de la hipertensión, optimizando el estado de los líquidos con diuréticos, y tratamiento de las enfermedades asociadas, como las alteraciones respiratorias durante el sueño. A pesar de que estos pacientes a menudo sufren disnea de esfuerzo, el ejercicio es seguro para ellos.
Control de la hiperpotasiemia. El control estrecho de la hiperpotasiemia es necesario para los pacientes tratados con antagonistas de la aldosterona. En estudios aleatorizados controlados, la eplerenona y la espironolactona disminuyeron notablemente la muerte y las rehospitalizaciones en pacientes con ICFEr. Como resultado, los antagonistas de la aldosterona recibieron una recomendación clase I en las guías de la ACCF/AHA.
No obstante, no se los adoptó tan rápidamente como a otros tratamientos debido al riesgo de hiperpotasiemia, en especial en pacientes de alto riesgo, como los que reciben antagonistas del sistema renina-angiotensina o los que padecen nefropatía crónica.
Sin embargo, en un estudio de Hernández et al con 5887 pacientes, el 18,2% fueron tratados con estos medicamentos, sin que se hallara diferencia en la mortalidad o en la rehospitalización por todas las causas. Aunque estos pacientes tuvieron menor riesgo de rehospitalización relacionada con su IC, también tuvieron 2,5 veces mayor riesgo de hospitalización por hiperpotasiemia dentro de los 30 días del inicio del tratamiento.
Estos datos, junto con los de estudios aleatorizados controlados indican que los antagonistas de la aldosterona pueden ser eficaces, pero se deben administrar con cautela en pacientes con antecedentes de hiperpotasiemia o insuficiencia renal (filtración glomerular estimada <60 ml/min). La potasiemia y la función renal se deben controlar en todos los pacientes, 1 semana, 4 semanas y 3 meses después de iniciado el tratamiento.
Tratamiento de resincronización cardíaca. El tratamiento de resincronización cardíaca (TRC) se debe considerar en pacientes con síntomas menos graves. En versiones anteriores de las recomendaciones de ACCF/AHA, la indicación clase I para TRC era sólo para pacientes con síntomas funcionales clase III de la New York Heart Association (NYHA), FE del 35% o menos y aQRS de 120 milisegundos o más.
En la actualización de 2012 de ACCF/AHA/Heart Rhythm Society, las indicaciones clase I se ampliaron a los pacientes con síntomas clase II de la NYHA, pero limitadas a pacientes con bloqueo de rama izquierda y QRS de 150 milisegundos o más. Estos cambios se efectuaron sobre la base de trabajos como REVERSE, MADIT-CRT y RAFT.
Tratamiento con hierro intravenoso. El tratamiento con hierro intravenoso mejora la capacidad de ejercicio en pacientes ferropénicos con IC. La anemia se asocia con mayor morbimortalidad entre los pacientes con IC. Debido a que la absorción oral del hierro no es buena, su eficacia y seguridad por vía intravenosa se investigaron en 3 estudios aleatorizados. El tratamiento con hierro intravenoso no tuvo efectos adversos y mejoró la clase funcional de la NYHA y la capacidad para el ejercicio en pacientes ferropénicos con IC con anemia y sin ella. La eritropoyetina se produce en los riñones, suele estar aumentada en pacientes con IC y se asocia con evolución desfavorable.
En pacientes con nefropatía crónica avanzada, la eritropoyetina se usa con frecuencia para tratar la anemia y por eso interesa su empleo en pacientes con IC y anemia. A pesar de resultados prometedores en estudios pequeños, el estudio reciente RED-HF (reducción de episodios con la darbepoyetina alfa en la IC) que aleatorizó a 1136 pacientes con hemoglobina de 9 -12 g/dl a recibir darbepoyetina alfa o placebo, no halló diferencia en la evolución clínica en ambos grupos. No hay hasta ahora datos suficientes para avalar el empleo sistemático de eritropoyetina en pacientes con IC y anemia.
Farmacogenética. La farmacogenética es el estudio de la función de los factores heredados en la respuesta de cada persona a un fármaco. Los adelantos actuales posibilitan la identificación rápida y con exactitud de la secuencia y la estructura del ADN. Como consecuencia, se puede relacionar la variación genómica con la respuesta al fármaco, lo que ayuda a pronosticar la variación individual de las respuestas a medicamentos específicos, a optimizar la elección y la dosis de los medicamentos y a evitar sus efectos adversos.
En la IC, un ejemplo de la posible importancia de la farmacogenética es el empleo de los β bloqueantes. Aunque éstos reducen la morbimortalidad, la respuesta es heterogénea. El subestudio de ADN de la investigación HF-ACTION halló que pacientes con una variante alélica específica del receptor adrenérgico β 1(Arg389) necesitaban dosis mayores de β bloqueantes para lograr efectos similares a los de otros pacientes. Aún quedan importantes desafíos a resolver sobre la implementación de la farmacogenética en la práctica clínica.