Introducción
Los años recientes han sido testigos de la expansión de los estudios de investigación, de grandes trabajos aleatorizados controlados y de nuevos tratamientos para las enfermedades pulmonares intersticiales (EPI) con la posibilidad de cambiar el panorama terapéutico para los pacientes. Para algunos de ellos, el objetivo será el control de los síntomas mientras que para otros puede ser la posibilidad de estabilizar la enfermedad o aun alcanzar su remisión.
¿Cuál es su frecuencia?
La fibrosis pulmonar idiopática (FPI) es la EPI más común, con una incidencia en el Reino Unido estimada en alrededor de 7,44/100.000 habitantes y una prevalencia estimada que varía desde 23,4 casos/100.000 habitantes en Europa hasta 63 casos/100.000 habitantes en EE. UU. Además de la FPI, la neumonitis por hipersensibilidad, la sarcoidosis y las enfermedades del tejido conectivo asociadas a la EPI constituyen la mayoría de los casos hallados en la práctica clínica diaria. Otras EPI como la proteinosis alveolar son raras (incidencia estimada: 1-2/millón de habitantes.
¿Cómo se clasifica?
Las EPI son un grupo heterogéneo de condiciones con diversos pronósticos y cuadros clínicos. Muchas se asocian con mayor morbilidad y mortalidad—por ej., la supervivencia de los pacientes con FPI es <3 años mientras que la neumonía intersticial aguda puede ser rápidamente fatal. Otras enfermedades, como la sarcoidosis pueden regresar sin tratamiento.
Es importante derivar cuanto antes al especialista, para confirmar el diagnóstico y el pronóstico y elegir la estrategia de manejo más apropiada. Sin embargo, un estudio de cohorte de pacientes con FPI identificó un lapso medio desde el comienzo de la disnea hasta la derivación al especialista de 2,2 años. Este retraso se asoció con mayor riesgo de muerte, independientemente de la gravedad de la enfermedad. El diagnóstico y la clasificación también afectan la posibilidad de entrar en muchos ensayos farmacológicos que actualmente están en ejecución.
La clasificación de las EPI es compleja, lo que refleja la diversidad de los factores causales subyacentes y los diferentes hallazgos histopatológicos. Aunque la mayoría de los trastornos se caracterizan por diversos grados de inflamación o fibrosis del intersticio pulmonar (la estructura del tejido conectivo de todo el pulmón), algunas como la neumonitis intersticial descamativa y la proteinosis alveolar se caracterizan por la ocupación del espacio aéreo. Algunas pueden ser principalmente inflamatorias, como la sarcoidosis, mientras que otras, como la FPI, son sobre todo fibróticas y pueden estar asociadas a una distorsión extensa de la arquitectura pulmonar y la pérdida de volumen.
La gama de factores causales atribuidos a las EPI incluye a las enfermedades del tejido conectivo y la exposición ambiental ocupacional como los trabajadores del al amianto, los fármacos tóxicos y la radiación. La FPI es la más común del grupo de las neumonías intersticiales idiopáticas, que son las EPI de etiología desconocida y se clasifican principalmente según los hallazgos histológicos.
| Clasificación simplificada de la enfermedad pulmonar intersticial |
| Neumonía intersticial (a menudo idiopática) • Fibrosis crónica-FPI crónica fibrosante, neumonía intersticial inespecífica idiopática • Aguda o subaguda-neumonía en organización, aguda o subaguda • Relacionadas con el tabaquismo-bronquiolitis respiratoria asociada a la EPI, neumonía intersticial descamativa |
| No clasificable Enfermedad del tejido conectivo asociada a la artritis reumatoidea, esclerodermia, dermatomiositis, polimiositis |
| Asociada a fármacos Metotrexato, bleomicina |
| Exposición inhalatoria Asbestosis, neumonitis por hipersensibilidad, neumoconiosis |
| Granulomatosa Sarcoidosis, neumonitis por hipersensibilidad |
| Síndromes hereditarios familiares y otras |
| Otras y condiciones raras Linfangioleiomiomatosis, histiocitosis de células de Langerhans |
El término alveolitis fibrosante criptogénica ya no se utiliza para describir la FPI. Algunos casos de EPI siguen siendo inclasificables a pesar de aplicar un enfoque multidisciplinario. En un estudio de cohorte se comprobó que el 10% de las EPI no se pudo clasificar y que los pacientes afectados tuvieron mejor pronóstico que los pacientes con FPI y un pronóstico comparable al de aquellos con enfermedad pulmonar fibrótica no idiopática.
¿Cómo se evalúa?
Aunque la disnea es un síntoma típico, para facilitar el diagnóstico precoz es necesario un elevado índice de sospecha clínica, ya que los pacientes suelen presentar signos y síntomas inespecíficos. En algunos casos, la EPI solo se puede sospechar después de un hallazgo incidental en una radiografía de tórax. No es infrecuente que antes de ser evaluados por el especialista los pacientes hayan recibido tratamiento para una infección o edema pulmonar. La falta de respuesta a los tratamientos para la infección o el edema pulmonar debe motivar la derivación inmediata al especialista para el diagnóstico de EPI.
Síntomas
En algunos casos, además de sugerir el diagnóstico de EPI, una historia detallada puede dar información suficiente para sospechar una presentación o causa específica de la enfermedad.
| Puntos clave de la historia para sospechar la EPI • Síntomas de la EPI: disnea, tos (a menudo seca) • Síntomas inespecíficos: fiebre, fatiga, pérdida de peso • Síntomas de enfermedad por reflujo gastroesofágico • Disfagia (enfermedad del tejido conectivo asociada a EPI) • Artralgias, rigidez matutina, sequedad ocular o bucal, alteraciones cutáneas, fenómeno de Raynaud, fotosensibilidad (enfermedad del tejido conectivo asociada a EPI) • Neurológico, erupciones (sarcoidosis, enfermedad del tejido conectivo asociada a EPI) • Síntomas oculares (enfermedad del tejido conectivo asociada a EPI, sarcoidosis) • Antecedentes familiares • Historia clínica-por ej., trastornos autoinmunes, enfermedad inflamatoria intestinal y trastornos renales como la poliangitis granulomatosa • Exposiciones, incluyendo medicamentos (por ej., nitrofurantoína, bleomicina, metotrexato), ocupación (por ej., trabajadores del metal, madera o amianto) y ambientales (por ej., aves) • Características personales de los pacientes, incluyendo la edad, el sexo y el consumo de tabaco |
Clásicamente, los pacientes presentan con disnea. La evolución de los síntomas desde su aparición puede ayudar a diferenciar el tipo de enfermedad. Algunas EPI, como la neumonía en organización o la neumonía intersticial aguda pueden tener un comienzo rápido, mientras que la evolución en el tiempo más habitual para muchas formas, como la FPI, es insidioso, con disnea que a menudo data de más de 1 año.
La edad también es importante. Algunas EPI, como la neumonitis por hipersensibilidad y la enfermedad del tejido conectivo asociada a EPI se presentan más frecuentemente en las personas <50 años. En la mayoría de los pacientes afectados, la sarcoidosis aparece entre los 25 y los 40 años, pero la enfermedad es poco común en las personas mayores; un estudio japonés halló una distribución bimodal, con un 30% de los casos ocurridos después de los 50 años. La FPI normalmente se presenta en pacientes de 60 a 70 años.
La tos es común en la EPI y a menudo es seca y exacerbada por el reflujo (implicado como factor causal de la EPI). Los pacientes pueden sentir malestar general y trastornos constitucionales, particularmente aquellos con enfermedad subyacente del tejido conectivo, vasculitis, y algunos casos de sarcoidosis.
Se debe interrogar acerca de las enfermedades del tejido conectivo relacionadas con síntomas del fenómeno de Raynaud, síntomas sicca (sequedad ocular y dificultad para tragar), esclerodactilia y artralgias. La hemoptisis es inusual y puede sugerir complicaciones como infección, embolia pulmonar, malignidad o vasculitis pulmonar.
Los pacientes con enfermedad del tejido conectivo conocida y aumento de los síntomas respiratorios deben ser derivados al neumonólogo. También es posible prevenir la enfermedad pulmonar de novo en pacientes sin características clínicas previas de enfermedad del tejido conectivo (por ej., la artritis reumatoide), de modo que es importante hacer una búsqueda activa de la condición, especialmente en los pacientes con signos de neumonía intersticial usual en la tomografía computarizada (TC); los síntomas articulares pueden desarrollarse más tardíamente.
El tabaquismo se asocia no solo con la FPI sino también con la EPI bronquiolitis respiratoria y oras EPI más raras como la histiocitosis de células de Langerhans y la neumonitis intersticial descamativa, así como es responsable del enfisema coexistente. Ensayos retrospectivos sugieren que el eflujo gastroesofágico contribuye a la patogénesis de la fibrosis. Los pacientes deben ser interrogados específicamente sobre los síntomas relacionados con la enfermedad por reflujo gastroesofágico, incluyendo el reflujo no ácido, lo que puede causar o exacerbar la EPI a través de episodios de aspiración recurrentes.
Fármacos y exposiciones
Es necesario obtener una historia detallada de los fármacos, las ocupaciones y las exposiciones.
| Factores ocupacionales y ambientales implicados en la neumonitis por hipersensibilidad |
| Ocupacionales • Son numerosas, incluyendo "el pulmón de los agricultores " (comúnmente actinomicetos termófilos o especies Aspergillus) y "pulmón de los aficionados a las aves " (buscar antígenos precipitantes de palomas, cotorras o loros). • Otras ocupaciones de alto riesgo son aquellas con exposición a animales (por ej. medicina veterinaria, agricultura); panaderos o trabajadores de los molinos, madera, fabricación o de papel, incluyendo MDF (tableros de fibra de densidad media); trabajadores textiles, pintura, plásticos ,o de la industria electrónica, o la exposición a productos químicos orgánicos aerosolizadas; y trabajadores del metal. • Asbesto-ocupaciones de alto riesgo como plomeros, electricistas, y trabajadores de la construcción, astilleros y trenes (la exposición puede haber ocurrido hace muchos años). |
| Ambiental • Inhalación de alérgenos en aerosol, agua en aerosol (por ej., piscinas, bañeras de hidromasaje, aire acondicionado, humidificadores). Los alérgenos incluyen los termoactinomicetos y Aspergillus, Klebsiella y especies de Acanthamoeba. • Ropa de cama de plumas; antes de adquirir edredones o almohadas de plumas se debe consultar. • Niveles elevados de moho húmedo en la casa o uso frecuente de compuestos de jardín (especie Aspergillus). |
| La toxicidad pulmonar se ha atribuido a una amplia variedad de medicamentos bajo receta y de venta libre así como a drogas ilícitas. Fármacos conocidos que causan toxicidad pulmonar • Agentes anti reumatoideos-metotrexato (puede ocurrir después de un cambio de dosis o de formulación, incluso en usuarios a largo plazo), oro, leflunamida, sulfasalazina, penicilamina • Agentes quimioterapéuticos-bleomicina, clorambucilo, inhibidores de la tirosinacinasa (por ej., imatinib), ciclofosfamida. • Agentes biológicos-factor de necrosis antitumoral (etanercept, infliximab). • Inhibidores selectivos de la recaptación de serotonina-citalopram, fluoxetina. • Antibióticos-nitrofurantoína, cefalosporinas. • Agentes cardiológicos: amiodarona, inhibidores de la enzima convertidora de angiotensina, estatinas. • Otros- talco, drogas ilícitas (por ej., cocaína; el talco utilizado para cortar muchas drogas), azatioprina, interferones |
Cualquier medicamento puede potencialmente causar toxicidad pulmonar. En caso de duda consultar en www.pneumotox.com
Los pacientes que comienzan a utilizar medicamentos nuevos con efectos adversos conocidos deben ser advertidos y evaluados para detectar el desarrollo de síntomas respiratorios. Los mecanismos incluyen el daño alveolar que progresa a la fibrosis (por ej., amiodarona, bleomicina), la hipersensibilidad (por ej., metotrexato) o la neumonía organizada (por ej., la nitrofurantoína). En algunos pacientes, la suspensión del fármaco responsable (y su sustitución adecuada cuando esté indicado) puede dar lugar a la resolución completa; ante la sospecha de EPI por esta causa se recomienda derivar al especialista.
Historia familiar
La patogénesis de las EPI es compleja, pero hay pruebas de que existe una estrecha interacción entre medio ambiente y factores genéticos. Están implicados algunos síndromes genéticos raros (como el síndrome de Hermansky-Pudlak); algunas EPI son más frecuentes en determinados grupos raciales (por ej., la sarcoidosis es más común en las personas de raza negra que en las de raza blanca), mientras que la EPI también puede ser familiar. La neumonía intersticial familiar queda definida cuando ≥2 miembros de la familia presentan neumonía intersticial idiopática. En más del 40% de estas familias, los miembros afectados tienen más de un tipo de fibrosis, lo que sugiere una susceptibilidad genética compartida. Al menos en el 20% de los casos de FPI existe un componente familiar.
Un beneficio del mayor conocimiento de la base genética de las EPI, en particular la FPI, es la posibilidad de contar con pruebas genéticas clínicas y un cribado prospectivo.
Examen
Un hallazgo semiológico habitual en las EPI es la auscultación de estertores crepitantes bilaterales al final de la inspiración, pero también se hallan otros signos auscultatorios. Por ej., la bronquiolitis de la neumonitis por hipersensibilidad presenta sibilancias inspiratorias y roncus.
Los pacientes con EPI quísticas como la histiocitosis de células de Langerhans y la linfangioleiomiomatosis pueden presentar signos de neumotórax y derrame pleural en aquellos con enfermedad del tejido conectivo asociada a EPI, la linfangioleiomiomatosis o, con menor frecuencia, a la sarcoidosis.
El frote pleural puede estar presente en los pacientes con artritis reumatoidea o lupus eritematoso sistémico. A pesar de ser una enfermedad grave, los pacientes con sarcoidosis suelen presentar pocos signos pulmonares. Hay muchos hallazgos extrapulmonares.
Más de la mitad de los pacientes con FPI tienen dedos en palillo de tambor, un signo que se asocia a una mala evolución, pero también se puede ver en otras EPI como la neumonitis intersticial descamativa, así como en complicaciones como el cáncer de pulmón. En los pacientes con sarcoidosis, los dedos en palillo de sugieren una fibrosis pulmonar grave progresiva. Un metaanálisis de os pacientes de raza blanca con enfermedad del tejido conectivo asociada a EPI halló una prevalencia elevada de hipertensión pulmonar, cuyos signos son las ondas a y v prominentes, un segundo ruido cardíaco aumentado y soplos de regurgitación mitral y tricuspídea.
Los pacientes pueden tener edema periférico. Algunos de las EPI se asocian con mayor riesgo de compromiso cardíaco, incluyendo la sarcoidosis (miocardiopatía y trastornos de la conducción) y la enfermedad del tejido conectivo asociada a EPI (miocarditis, pericarditis, derrame pericárdico). Numerosos hallazgos cutáneos se asocian con la enfermedad del tejido conectivo y enfermedades reumatológicas, que son reconocidas causas de fibrosis. El e eritema nodoso se asocia con sarcoidosis, la erupción heliotropo con la dermatomiositis y la calcinosis con la esclerodermia.
| Características clave para la exploración clínica de la EPI • Crepitantes bibasales al final de la inspiración (fibrosis) • Crepitaciones inspiratorias (neumonitis por hipersensibilidad) • Dedos en palillo de tambor • Derrame pleural (enfermedades del tejido conectivo, linfangioleiomiomatosis, sarcoidosis) • Hipertensión pulmonar (especialmente, enfermedades del tejido conectivo- onda v, soplos de regurgitación tricuspídea o pulmonar, edema periférico • Artritis (enfermedad del tejido conectivo o sarcoidosis) • Piel-eritema nudoso (sarcoidosis), fenómeno de Raynaud/esclerodactilia/telangiectasia (esclerosis sistémica) • Linfadenopatía y hepatoesplenomegalia (sarcoidosis) • Signos neurológicos (sarcoidosis, vasculitis y enfermedades del tejido conectivo) • Signos oculares (sarcoidosis, enfermedades del tejido conectivo) |
¿Cómo se investigan?
Investigaciones iniciales
Los pacientes con sospecha de EPI deben ser derivados al especialista, pero antes, y para facilitar un diagnóstico y evaluar las complicaciones antes mencionadas se pueden solicitar varios estudios. Los análisis de sangre de rutina pueden dar pruebas de inflamación o de factores complicantes, como la hipercalcemia en la sarcoidosis. Como pruebas iniciales, la guía de la British Thoracic Society sugiere un análisis de sangre completo, urea y electrolitos, pruebas de función hepática, calcemia, velocidad de sedimentación globular y proteína C reactiva. Otras pruebas dependerán del contexto clínico y las características clínicas de la EPI.
Ante la sospecha de vasculitis, es útil el análisis de orina. La espirometría realizada en la comunidad puede revelar un defecto pulmonar restrictivo. Sin embargo, muchos pacientes con enfisema también desarrollan fibrosis, y a causa de las fisiologías contrastantes la espirometría puede ser normal u obstructiva, lo que por sí solo no debería restar valor a la sospecha diagnóstica. Los pacientes con enfisema y fibrosis combinados son más propensos a desarrollar hipertensión pulmonar.
Investigación radiológica
Radiografía de tórax
La radiografía de tórax suele ser el primero estudio radiológico solicitado. Aunque no es sensible ni específica, no se puede obviar su realización, ya que es una herramienta sencilla que puede identificar signos que orientan sobre la condición subyacente. La revisión de las radiografías anteriores puede ayudar a determinar si los cambios son agudos o crónicos.
Los patrones de la enfermedad, como la predominancia en la parte superior o inferior de los pulmones puede sugerir condiciones particulares, pudiendo también hallarse signos de factores causales subyacentes como las placas pleurales de asbesto. La radiografía de tórax puede ayudar a excluir el edema o la infección y puede detectar complicaciones, incluyendo las malignidades. Los hallazgos típicos de FPI incluyen la reducción del reticulado y de los volúmenes pulmonares.

Tomografía computarizada de alta resolución
Actualmente, esta tomografía es una investigación estándar en los pacientes con sospecha de EPI. En algunos casos en los que la historia es compatible, puede confirmar el diagnóstico, evitando la necesidad de la broncoscopia o la biopsia pulmonar. La FPI provoca un patrón de fibrosis de "neumonía intersticial usual" asociada con lesiones en panal de abeja (dilataciones quísticas de los bronquiolos distales, secundarias a la destrucción fibrótica de los espacios aéreos adyacentes).
La neumonía intersticial usual no es específica de la FPI y se puede ver en otras EPI, como las enfermedades del tejido conectivo asociadas a EPI, la asbestosis y la sarcoidosis. Las características clínicas y los hallazgos radiológicos como el derrame pleural, las placas de la asbestosis o la dilatación esofágica de la escleroodermia pueden diferenciar las causas subyacentes.
En una TC de alta resolución, los radiólogos pueden describir diferentes patrones de la neumonía intersticial usual: típico, posible y atípico, lo que puede ayudar en la toma de decisiones.

Otras investigaciones especializadas
Se deben hacer pruebas de la función pulmonar incluyendo la medición de la difusión de gases, cuyos resultados seriados son útiles para evaluar la respuesta al tratamiento o el deterioro. Estas pruebas suelen ser más esclarecedoras que la evaluación del volumen pulmonar estático. El patrón típico de las pruebas de función pulmonar en las EPI es el restrictivo, pero algunos fumadores pueden tener enfermedad de la vía aérea coexistente y su patrón restrictivo es poco frecuente. Los pacientes con sarcoidosis pueden tener un patrón obstructivo por compromiso endobronquial.
La medición de la difusión de gases basal identifica a los pacientes con FPI de mal pronóstico. El resultado de la caminata de 6 minutos brinda un buen indicio basal para la rehabilitación pulmonar y el resultado a largo plazo de la FPI. Otras investigaciones están destinadas a confirmar o descartar el diagnóstico presuntivo. Los análisis serológicos determinan las respuestas alérgicas en la neumonitis por hipersensibilidad o la enfermedad del tejido conectivo emergente.
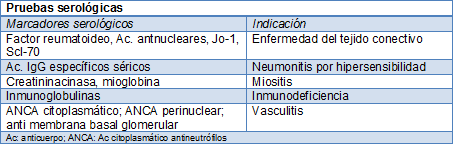
Las pruebas de provocación para la neumonitis por hipersensibilidad no están estandarizadas y generalmente no son necesarias.
¿Cómo se confirma el diagnostico?
El estándar actual para el diagnóstico de EPI es la intervención de un equipo multidisciplinario integrado por neumonólogo, radiólogo, anatomopatólogo, especialista torácico y enfermeras especializadas. El diagnóstico típico está basado en la confirmación de la EPI, ya que siempre que sea posible hay que establecer un diagnóstico, sobre todo para determinar las causas subyacentes y el estadio de la enfermedad, y discutir los objetivos terapéuticos.
Algunas condiciones de los pacientes son más complejas, y a pesar del conocimiento del equipo multidisciplinario, no siempre se puede arribar a un diagnóstico seguro. En este caso se deben considerar los riesgos y beneficios de obtener muestras mediante la broncoscopia o la biopsia pulmonar quirúrgica. Es necesario que, en lo posible, el equipo arribe al diagnóstico de EPI para decidir acerca de las estrategias terapéuticas. No todos los casos requieren la confirmación histológica, particularmente si la opinión clínica y radiológica coincide. La mayor edad se asocia con mayor probabilidad de FPI.
Broncoscopía
La broncoscopía permite tomar muestras para excluir la infección, Identificar las diferentes células y permitir biopsias endobronquiales de pequeño volumen o, las biopsias transbronquiales para su posterior examen histológico. En general, la broncoscopía es segura, mientras que las principales complicaciones de la biopsia transbronquial son el neumotórax o el sangrado.
Mediante el lavado broncoalveolar se pueden observar células diferenciales que generalmente no solo son diagnósticas sino que también pueden apoyar el diagnóstico de neumonitis por hipersensibilidad o sarcoidosis, en el caso de hallarse linfocitosis; también pueden ser examinadas para buscar células malignas.
La American Thoracic Society sugiere el uso de de la TC de alta resolución para elegir el sitio apropiado de la biopsia. Las biopsias endobronquial o transbronquial son útiles para establecer el diagnóstico de sarcoidosis. Estas muestras son demasiado pequeñas para hacer la clasificación histológica de otras EPI y en presencia de fibrosis establecida tienen un valor limitado. La biopsia transbronquial no está indicada para descartar o confirmar la FPI. Sin embargo, en algunos casos, el lavado broncoalveolar puede ser importante para diferenciarla de la neumonitis por hipersensibilidad crónica.
Biopsia quirúrgica
La biopsia quirúrgica del pulmón permite obtener una muestra que brinda un diagnóstico del tipo específico de EPI, aunque hay problemas con la variabilidad interobservador e intraobservador, incluso entre los anatomopatólogos expertos, y al considerar la selección de los pacientes ésto debe ser tenido en cuenta. Los beneficios se deben comparar con los riesgos, especialmente en los pacientes propensos al compromiso respiratorio, las exacerbaciones, la hipertensión pulmonar y otras comorbilidades.
Un metaanálisis mostró tasas de mortalidad de 4,3% a los 30 días para la biopsia pulmonar a cielo abierto y del 2,1% para la biopsia quirúrgica toracoscópica video asistida. Esto significa que se necesita una cuidadosa deliberación antes de recomendar una biopsia quirúrgica del pulmón. La mortalidad aumenta con la edad. Sin embargo, en algunas formas de EPI, sin la biopsia quirúrgica la confirmación no es posible.
¿Cómo se trata?
Los objetivos del tratamiento varían dependiendo del comportamiento clínico de la EPI. En muchas EPI tales como la FPI, el objetivo será frenar o estabilizar la progresión de la enfermedad. Otras EPI, como la bronquiolitis respiratoria asociada a EPI, son autolimitadas y potencialmente reversibles.
En los pacientes con enfermedad inclasificable, que representa alrededor del 10% de la cohorte de EPI, el equipo multidisciplinario tiene que llegar a un diagnóstico de trabajo y usar esto para determinar un enfoque pragmático para el tratamiento y el seguimiento. Los planes terapéuticos también deben incluir terapias de apoyo, incluyendo la rehabilitación pulmonar, el alivio sintomático (por ej., tos, ansiedad), y el oxígeno suplementario.
Terapéutica
A continuación se expone una breve información sobre el manejo de las EPI específicas.
Fibrosis pulmonar idiopática
La FPI constituye más de la mitad de los casos de EPI en la práctica clínica y tiene peor pronóstico que muchas enfermedades malignas. Los tratamientos previos como los esteroides, la ciclofosfamida, el tratamiento triple (prednisolona, azatioprina y N-acetilcisteína), o la N-acetilcisteína sola han mostrado ser ineficaces o peligrosos. Un estudio aleatorizado controlado de N-acetilcisteína no mostró beneficios al compararla con el placebo para el tratamiento de la FPI. Estas opciones ya no se recomiendan. Sin embargo, la N-acetilcisteína y otros mucolíticos a veces son utilizados como expectorantes.
Ciertos pacientes pueden beneficiarse participando de ensayos farmacológicos para opciones terapéuticas nuevas, las cuales pueden ayudar a enlentecer la velocidad de la inexorable declinación de la FPI. Actualmente, en el Reino Unido, el único tratamiento aprobado por el National Institute for Health and Care Excellence for idiopathic pulmonary fibrosis (NICE) es la pirfenidona. Este instituto recomienda su uso en los pacientes con una capacidad vital forzada esperada de 50-80%. Es costosa, requiere el monitoreo de la función pulmonar y sus efectos colaterales incluyen náusea, dispepsia, fatiga y fotofobia.
Trabajos aleatorizados y controlados han comprobado que no revierte la fibrosis establecida pero enlentece la velocidad de la declinación de la función pulmonar y reduce algo la mortalidad global, a juzgar por la evidencia surgida de estudios clínicos recientes. De acuerdo con la guía de NICE, ampliamente adoptada, el tratamiento debe ser suspendido cuando la función pulmonar declina ≥10% en 1 año, en relación con la cifra basal.
El nintedanib, un inhibidor de la tirosinacinasa intracelular, con propiedades antifibróticas y antiinflamatorias, ha sido aprobado recientemente pero todavía no ha sido aceptado por NICE mientras que los trabajos clínicos también muestran que enlentece la declinación de la función pulmonar, del mismo modo que la pirfenidona. El efecto colateral principal es la diarrea, los anticoagulantes están contraindicados y es necesario monitorear la función pulmonar. Otros fármacos están en la fase 2b de la investigación (simtuzimab, lebrikizumab), lo que despierta esperanzas para el futuro tratamiento clínico de la FPI.
Trastorno del tejido conectivo asociado a la enfermedad pulmonar intersticial
La participación del pulmón en las enfermedades del tejido conectivo va desde la fibrosis hasta la enfermedad vascular pulmonar, la vasculitis y las complicaciones pleurales. A pesar de la considerable carga de complicaciones pulmonares de la enfermedad del tejido conectivo, el tratamiento de la enfermedad asociada a la EPI no está avalado por evidencia contundente. Los únicos ensayos controlados aleatorizados se refieren al uso de la ciclofosfamida en la esclerodermia. Uno de ellos mostró un modesto efecto significativo sobre la función pulmonar y calidad de vida relacionada con la salud. Aunque en el otro estudio no se halló una mejoría significativa, hubo una tendencia a la mejoría de la capacidad vital forzada, y el tratamiento fue bien tolerado.
Los agentes de elección son los inmunosuupresores. A pesar de sus riesgos, la evidencia base para su uso es mínima, con pocos datos para guiar la iniciación y duración del tratamiento óptimo.
Los corticosteroides y agentes ahorradores de esteroides, como la azatioprina y el micofenolato, se utilizan generalmente en la enfermedad leve, con ciclofosfamida para los casos más graves o refractarios. La EPI inducida por fármacos es un problema en la enfermedad del tejido conectivo asociada a la EPI, ya que, casi todos los fármacos utilizados para tratar la enfermedad el tejido conectivo subyacente pueden causar EPI. Las reacciones pueden variar desde infiltrados y empeoramiento de la fibrosis subyacente, hasta el daño alveolar agudo, potencialmente mortal. Se requiere un elevado índice de sospecha y una estrecha vigilancia.
Sarcoidosis
La sarcoidosis es una condición multisistémica, granulomatosa, inflamatoria, que se presenta típicamente en los adultos más jóvenes, y no son inusuales los síntomas extratorácicos como el eritema nudoso. Tiene predilección por el aparato respiratorio-en una gran cohorte americana, el tórax estaba involucrado en más del 90% de los casos. Los pacientes pueden pasar de la etapa 1 de la enfermedad (solo linfadenopatías bihiliares) a la etapa 2 o más (participación del parénquima pulmonar) sin saber que están afectados por la sarcoidosis. Hasta un 10% puede progresar a la fibrosis.
La etapa 1 de la sarcoidosis se manifiesta típicamente con adenopatías bihiliares y adenopàtías paratraqueales derechas (tríada de Garland). En las etapas 2 y 3, la infiltración granulomatosa del pulmón lleva a la formación de nódulos perilinfáticos. Hasta el 10% de los casos progresa a la fibrosis (etapa 4). El grado y el tipo son más variables que en la FPI.
La guía de la British Thoracic Society indica que la etapa 1, asintomática, no requiere tratamiento, como tampoco los estadios 2 y 3 asintomáticos que solo tienen una anormalidad leve de la función pulmonar.
Como tratamiento de primera línea para la progresión o los síntomas de la sarcoidosis, desde la década de 1950 se utilizan los esteroides. La imposibilidad de minimizaar la dosis, los efectos colaterales o la falta de respuesta pueden motivar el uso alternativo de inmunosupresores, pero falta evidencia al respecto. El agente ahorrador de esteroides más comúnmente utilizado es el metotrexato, con tasas de respuesta de hasta el 60%.
Otros son la azatioprina, la hidroxicloroquina o los inhibidores del factor de necrosis tumoral α, como el infliximab para la enfermedad recalcitrante. Los corticosteroides inhalados pueden ayudar a controlar la tos o la enfermedad de las vías aéreas, y evitar ciertos efectos colaterales asociados a las dosis más elevadas de esteroides. Una revisión sistemática mostró que los efectos son pequeños y los resultados no concluyentes.
Neumonitis por hipersensibilidad
La neumonitis por hipersensibilidad (alveolitis alérgica extrínseca) puede ocurrir a cualquier edad y se debe a la exagerada respuesta inmunológica a la inhalación de antígenos. Puede presentarse en forma aguda, subaguda y crónica—el 20% de las EPI se debe a la neumonitis por hipersensibilidad crónica.
El manejo incluye la identificación y eliminación del agente sensibilizante, lo que puede ser obvio pero suele ser difícil de identificar y todavía más difícil es eliminar los alérgenos, especialmente los agentes ambientales ubicuos. A menudo, cuando no se puede contrarrestar o eliminar el posible alérgeno y cuando hay deterioro funcional, los síntomas son controlados mediante los esteroides, No hay trabajos controlados sobre el manejo de la neumonitis por hipersensibilidad crónica. La ciclofosfamida intravenosa puede ser efectiva y hay informes de casos con buenos resultados usando agentes biológicos para los casos refractarios.
Rehabilitación pulmonar
Hay suficiente evidencia de que la rehabilitación pulmonar ayuda a los pacientes disneicos. Un metaanálisis confirmó el beneficio de la rehabilitación pulmonar en los pacientes con EPI. En un estudio aleatorizado y controlado, los pacientes obtuvieron una mejoría significativa en la distancia recorrida durante 6 minutos. Lamentablemente, dicen los autores, la rehabilitación pulmonar no está universalmente disponible en muchas regiones y está restringida a los pacientes con EPOC, en quienes los efectos son más conocidos y bien documentados. Los beneficios se observan en la mejoría de la fuerza y la aptitud de la musculatura no respiratoria, lo que contribuye a mejorar las distancias recorridas. También se puede ofrecer apoyo psicosocial, consejo nutricional y recomendar el abandono del cigarrillo
Trasplante de pulmón
El trasplante de pulmón mejora la supervivencia en casos muy bien seleccionados. Tiene por objeto mejorar la supervivencia y la calidad de vida; el pronóstico de supervivencia sin trasplante es <50% a los 5 años. El 23% de los trasplantes de pulmón se realiza en pacientes con FPI. Las enfermedades del tejido conectivo abarcan <4% de su indicación, mientras que en otras EPI el porcentaje es menor.
La elección de los pacientes es importante, y las guías recomiendan la derivación de los pacientes con FPI que tienen una reducción de la capacidad vital forzada ≥10% en 6 meses y un disminución de la saturación de oxígeno <89%, o que requieren oxígeno en reposo.
Un estudio retrospectivo de 105 pacientes con FPI, realizado en un solo centro, comprobó que los pacientes que tenían este grado de desaturación tuvieron una supervivencia a los 5 años del 20% comparada con el 60% en los pacientes sin desaturación. En los pacientes sin FPI, se considera el trasplante cuando la capacidad vital forzada es <50% o hay hipoxemia (presión parcial de oxígeno <55 mm Hg).
La International Society of Heart and Lung Transplantation sugiere un máximo de edad de 65 años, aunque los resultados basados en el registro de EE. UU. muestran una mejoría en el injerto y la supervivencia en pacientes que superan esa edad. Las contraindicaciones también incluyen la infección micobacteriana, el tabaquismo y el uso indebido de sustancias sin abstinencia prolongada, malignidad reciente, daño orgánico no respiratorio mayor intratable y obesidad.
La mitad de los pacientes con FPI recibe el trasplante pulmonar bilateral. La mortalidad a los 3 meses, no ajustada. de los pacientes con FPI es 15%, y entre los que sobreviven 1 año, la supervivencia a los 5 años es del 60%. Los pacientes mejoran notablemente la función pulmonar y las actividades de la vida diaria. Uno cada 6 pacientes en lista de espera para el trasplante muere antes de haber hallado al donante del órgano
¿Cuáles son las consideraciones para la atención al final de la vida?
El manejo de los pacientes con EPI (en particular la FPI) abarca mucha atención al final de la vida. Algunos pacientes se presentan demasiado tarde para hacer un tratamiento antifibrótico, y todo lo que se puede hacer es brindar apoyo para el manejo de los síntomas. Es importante considerar desde el principio las expectativas del paciente, incluso de aquellos en los que está indicado un tratamiento específico, ya que los efectos de los tratamientos siguen siendo escasos en la mayoría de ellos.
Los pacientes sufren una gran limitación derivada de la disnea y muchos son muy conscientes del pronóstico. Es necesario dar explicaciones cuidadosas, proveer literatura específica sobre la enfermedad, y ofrecer el apoyo de los especialistas. El apoyo de la enfermería especializada es primordial para estos pacientes y cada vez se están formando más grupos de apoyo, como la British Lung Fundation y organizaciones benéficas como Action for Pulmonary Fibrosis en el Reino Unido.
La participación temprana de equipos como los de terapeutas ocupacionales ayuda con los problemas prácticos que rodean al mantenimiento de la independencia (por ej., la instalación de ascensores, escaleras y pasamanos), siendo de vital importancia los equipos de enfermería en la comunidad y los especialistas en cuidados paliativos.
El apoyo de la movilidad también es importante, por ej., sillas o scooters eléctricos y símbolos de libre estacionamiento para discapacitados. Para las personas sin diagnóstico de cáncer, en algunas zonas existen albergues y el apoyo necesario de especialistas en cuidados paliativos, que pueden ser muy valiosos en la etapa terminal de la enfermedad. Los pacientes deben tener tiempo para considerar sus deseos del final de la vida, incluyendo la toma de decisiones sobre el ingreso hospitalario y el estado de la reanimación, de la misma manera que aquellos con otras condiciones que limitan la vida.
| Puntos principales • Las EPI son un grupo complejo de trastornos, pero la FPI, la neumonitis por hipersensibilidad, la enfermedad del tejido conectivo asociada a EPI y la sarcoidosis son las más vistas en la práctica clínica. • Los pacientes presentan signos y síntomas inespecíficos y por lo tanto se requiere un alto índice de sospecha. • El hallazgo típico de crepitaciones bibasales se puede confundir con el edema pulmonar, pero los pacientes por lo general carecen de las otras características de éste. La falta de respuesta al tratamiento para el edema o la infección debe despertar la sospecha de EPI. • La derivación precoz al especialista permite el diagnóstico y el tratamiento rápido para optimizar los resultados; este proceso puede ser facilitado por las investigaciones en la comunidad, incluyendo la radiografía de tórax y algunos estudios serológicos. • El control de los síntomas, la terapia ocupacional y los cuidados paliativos también son aspectos importantes del manejo de los pacientes. |
*Traducción y resumen objetivo: Dra. Marta Papponetti