|
Pontos importantes
|
Introdução
Embora os médicos tenham tratado a pneumonia por séculos, cada estágio do processo de tomada de decisão clínica ainda apresenta desafios, desde a determinação do ambiente de tratamento mais adequado para um paciente com suspeita de pneumonia até o planejamento do acompanhamento após o término do antibiótico. Ao longo dos anos, os médicos testemunharam o advento de novas terapias médicas e respiratórias, bem como o desenvolvimento de resistência aos antibióticos no tratamento dessa infecção comum.
Pacientes hospitalizados com pneumonia se enquadram em 2 categorias: aqueles com pneumonia adquirida na comunidade (PAC) e aqueles que desenvolvem pneumonia adquirida em hospital ou associada à ventilação mecânica enquanto já estão hospitalizados.
Cada população de pacientes enfrenta exposições únicas de organismos e, portanto, os testes de diagnóstico recomendados, os regimes de tratamento empírico e as metas para a prevenção de infecções variam.
Este artigo revisa as diretrizes da Infectious Diseases Society of America (IDSA) e da American Thoracic Society (ATS) 1 e interpreta estudos recentes para abordar as questões que surgem especificamente no tratamento hospitalar da PAC.
Estratificação de risco para pneumonia adquirida na comunidade
As diretrizes 1 da IDSA / ATS de 2019 enfatizam a importância de determinar primeiro qual nível de atendimento ao paciente é necessário: O tratamento ambulatorial é adequado ou o paciente precisa ser internado no hospital ou mesmo na unidade de terapia intensiva?
A triagem adequada pode evitar o estresse do paciente e do sistema de saúde associado à subestimação ou superestimação da gravidade da doença.
Pacientes com alto risco de morte, cuja acuidade não é totalmente avaliada, enfrentam suporte inadequado, enquanto aqueles admitidos, apesar do baixo risco de morte, podem estar desnecessariamente sujeitos a riscos do ambiente hospitalar, como infecções por organismos multirresistentes associado à saúde.
As calculadoras de risco são usadas rotineiramente para ajudar os médicos a avaliar seus pacientes na prática diária, embora não sejam especificamente validadas para prever a necessidade de internação.
CURB-65 é uma calculadora simples baseada em 5 fatores de risco. Os pacientes recebem um ponto para cada confusão, nitrogênio ureico alto no sangue azoto, alta taxa respiratória, baixa pressão sanguínea (do inglês low blood pressure) ou idade igual ou maior que 65 anos, quanto maior o escore, maior o risco de mortalidade no 30º dia.
De acordo com a IDSA / ATS, os pacientes com pontuação 0 ou 1 podem ser tratados ambulatorialmente, aqueles com pontuação 2 devem ser internados no hospital e aqueles com pontuação 3, 4 ou 5 precisam de cuidados em unidade de terapia intensiva. ( Nota do editor: você pode encontrar uma versão online desta calculador clicando aqui)
Uma versão abreviada desta calculadora, CURB-65, permite estratificação de risco para pacientes ambulatoriais sem trabalho laboratorial. 1
O Índice de Gravidade da Pneumonia incorpora 20 fatores de risco para colocar os pacientes em 5 classes correlacionadas com o risco de mortalidade 5 .
Os autores sugerem gerenciamento ambulatorial para aqueles nas classes I ou II e gerenciamento hospitalar para aqueles nas classes de risco IV e V. Os pacientes na classe III podem ser tratados com segurança em um ambiente ambulatorial com suporte adequado ou em uma unidade de observação de pacientes internados.
As diretrizes IDSA / ATS listam um conjunto separado de critérios maiores e menores para definir "pneumonia grave" para determinar quais pacientes com suspeita de PAC precisam de tratamento intensivo. 1 Pelo menos 1 dos critérios principais ou pelo menos 3 dos critérios secundários são necessários para o diagnóstico de pneumonia grave (ver tabela abaixo).

Uma revisão retrospectiva de mais de 1.800 pacientes descobriu que 45% dos pacientes que tinham PAC de "baixo risco" no Índice de Gravidade da Pneumonia foram admitidos. 7 Pacientes com comprometimento cognitivo, doença coronariana, diabetes mellitus, doença pulmonar, opacidades radiográficas multilobulares, oxigenoterapia domiciliar, uso de corticosteroides ou uso de antibióticos antes da apresentação tinham maior probabilidade de serem hospitalizados.
Os autores enfatizam que o julgamento clínico deve ser aplicado aos resultados de qualquer uma dessas calculadoras para classificar adequadamente os pacientes com pneumonia.
Diagnóstico de pneumonia adquirida na comunidade
Depois de submeter um paciente com suspeita de PAC ao nível de cuidado mais seguro, vários métodos radiográficos e laboratoriais podem ser usados para verificar o diagnóstico e identificar o organismo mais provável responsável pela infecção em curso.
Radiografias de tórax com infiltrados demonstráveis são necessárias para diagnosticar PAC e distingui-la da infecção respiratória superior. 1
Diferentes organismos com padrões de infiltração característicos podem estar associados, muitas vezes se manifestando dentro de 12 horas após o início dos sintomas:
Pneumonia focal não segmentar ou lobar (Fig. 1)
Pneumonias bacterianas típicas causadas por organismos como Streptococcus pneumoniae tendem a se apresentar com opacidade de 1 segmento ou lóbulo do espaço aéreo, embora o uso de antibióticos possa alterar sua fisiopatologia para criar um padrão multilobular irregular de opacidade.
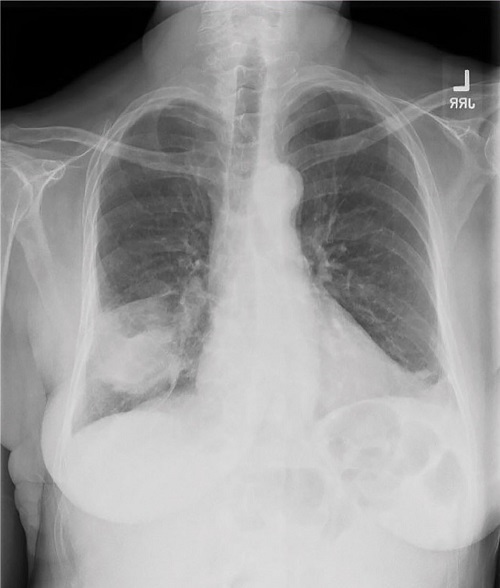
Figura 1.Pneumonia lobar focal.
Broncopneumonia multifocal ou pneumonia lobar
A broncopneumonia, caracterizada de forma semelhante por um padrão irregular, é mais comumente causada por Staphylococcus aureus, Haemophilus influenzae e fungos. 8
Pneumonia "intersticial" focal ou difusa (Fig. 2)
Organismos bacterianos atípicos, incluindo Legionella pneumophila, Mycoplasma pneumoniae e Chlamydophila pneumoniae, frequentemente envolvem as bases pulmonares em um padrão reticulonodular bilateral difuso, mas podem começar como opacidades lobulares isoladas na radiografia de tórax. 9 Os organismos virais também estão associados ao envolvimento pulmonar difuso e bilateral.
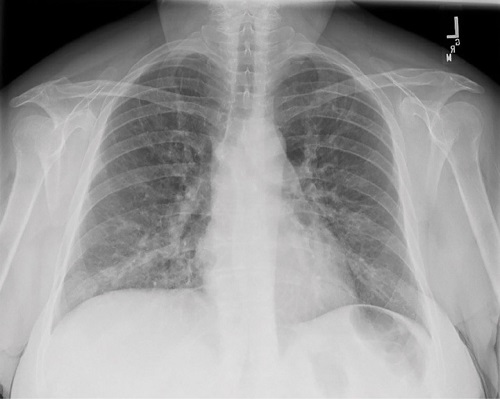
Figura 2. Pneumonía intersticial difusa.
A identificação radiográfica precoce de complicações pulmonares, como derrames pleurais ou lesões cavitantes, pode fornecer mais pistas sobre o organismo causador e permitir uma intervenção oportuna. 9
Quão precisa é a radiografia do tórax?
A utilidade das radiografias de tórax no diagnóstico de PAC está sujeita à variabilidade interobservador, com alguns estudos citando 65% de acurácia no diagnóstico de pneumonia viral, 67% no diagnóstico de pneumonia bacteriana e nenhuma confiabilidade estatística para diferenciar pneumonia bacteriana de não bacteriana.
Microbiologia
Um histórico social abrangente deve ser coletado de cada paciente com suspeita de PAC para detectar possíveis exposições ocupacionais, de viagem ou endêmicas. Isso orientará os testes microbiológicos e o tratamento empírico com antibióticos.
Por exemplo, os pacientes que se apresentam durante a temporada de gripe ou com exposições conhecidas a aves em áreas de surtos de influenza anteriores devem ser rastreados para influenza A e B com um esfregaço nasofaríngeo.
O isolamento de um organismo específico em pacientes ambulatoriais com PAC pode não ser necessário, mas é recomendado para orientar a redução de esquemas antibióticos empíricos. 1 Antes do tratamento, a coloração de Gram e a cultura devem ser realizadas em pacientes capazes de expectorar adequadamente uma amostra de boa qualidade ou por aspirado endotraqueal em pacientes intubados.
Os pacientes que atendem aos critérios para pneumonia grave definidos pelas diretrizes da IDSA / ATS merecem hemocultura e cultura de escarro, bem como teste de antígeno urinário para L. pneumophila e S. pneumoniae. 1
Teste de procalcitonina
O teste de procalcitonina pode ajudar a diferenciar patógenos virais de bacterianos em pacientes internados para PAC, evitando o uso de antibióticos desnecessários e permitindo uma redução rápida na terapia empírica de forma mais eficaz do que o julgamento clínico sozinho. 13
Embora qualquer pneumonia infecciosa possa precipitar elevações neste biomarcador sérico, bactérias típicas tendem a produzir níveis mais elevados de procalcitonina do que bactérias ou vírus atípicos. 14
As citocinas, associadas a infecções bacterianas, aumentam a liberação de procalcitonina, enquanto os interferons, associados a infecções virais, inibem a liberação de procalcitonina. No entanto, este biomarcador não é perfeito e não aumentará em até 23% das infecções bacterianas típicas. 14
Por esse motivo, os autores afirmam que a procalcitonina não deve substituir o julgamento clínico ao orientar a decisão de iniciar a terapia antimicrobiana para pacientes com suspeita de PAC, mas pode ser usada em conjunto com o julgamento clínico para reduzir a terapia.
Em pacientes cujos registros médicos sugerem causas alternativas de dificuldade respiratória ou melhora com terapias administradas concomitantemente, como diurese, uma procalcitonina negativa pode ajudar a orientar a descontinuação dos antibióticos.
Por outro lado, em pacientes com influenza comprovada por PCR, uma procalcitonina elevada pode sugerir a continuação de antibióticos para tratar a superinfecção bacteriana.
Gestão de PAC
Terapia antibiótica
A seleção de antibióticos antes de identificar um patógeno causador deve ser feita com base nos fatores de risco e no grau de doença do paciente.

A doxiciclina pode ser usada como alternativa ao macrolídeo ou à fluoroquinolona respiratória para cobrir organismos atípicos como Chlamydia pneumoniae, Legionella pneumophila e Mycoplasma pneumoniae em pacientes com QTc prolongado. Em pacientes alérgicos à penicilina, o aztreonam deve ser usado em combinação com um aminoglicosídeo e uma fluoroquinolona respiratória.
Pacientes que podem ter sido expostos à gripe ou que têm histórico de uso de drogas injetáveis ou doença pulmonar estrutural ou que têm um abscesso pulmonar, infiltrados cavitários ou obstrução endobrônquica também devem ter cobertura contra S. aureus resistente à meticilina (MRSA) adquirido na comunidade com vancomicina ou linezolida.

Se um organismo for identificado por cultura, PCR ou sorologia, o regime empírico de antibióticos deve ser adaptado para esse organismo.
A triagem de MRSA nas narinas pode ser usada de forma confiável para guiar regimes antimicrobianos empíricos e direcionados; os pacientes que começaram a tomar vancomicina ou linezolida com base nos fatores de risco mencionados acima podem ser reduzidos com segurança com base em um esfregaço nasal negativo. 15
O antígeno urinário pneumocócico tem um valor preditivo negativo igualmente confiável e pode ser usado para reduzir a terapia antimicrobiana empírica. 16
No caso de a avaliação microbiológica não identificar um organismo causador, os fatores de risco individuais do paciente listados acima devem ser considerados na redução da terapia para um regime final com cobertura para MRSA, Pseudomonas aeruginosa ou patógenos atípicos, conforme apropriado.
A pneumonia por Pseudomonas foi associada a um maior risco de mortalidade e recidiva do que a pneumonia causada por outros patógenos.
As diretrizes da IDSA / ATS recomendam não usar corticosteroides para o tratamento, exceto em pacientes com choque séptico refratário.
Post management
Os pacientes que estão hemodinamicamente estáveis, que podem ingerir medicamentos com segurança e têm um trato gastrointestinal normal podem receber alta da terapia oral sem esperar a resposta clínica.
Os antibióticos devem ser administrados por pelo menos 5 dias, embora períodos mais longos possam ser necessários em pacientes imunocomprometidos ou com complicações pulmonares ou extrapulmonares. 1
Uma consulta de infectologia pode ser benéfica se a terapia antibiótica intravenosa de longo prazo for prevista ou se o paciente piorar progressivamente com a terapia antimicrobiana baseada em diretrizes.
A consulta com a pneumologia para broncoscopia pode ser necessária para obter amostras respiratórias profundas, especialmente se o paciente estiver piorando clinicamente e o patógeno causador permanecer não identificado.
Os autores reconhecem que o desempenho da broncoscopia e amostras de lavagem broncoalveolar é reduzido com uma maior duração da terapia antibiótica, mas eles acreditam que no contexto de piora clínica apesar dos antibióticos, o lavado broncoalveolar pode ajudar a identificar com sucesso patógenos multirresistentes ou atípicos que podem não estar cobertos pelo esquema antibiótico atual.
A consulta com pneumologia também é indicada para pacientes com complicações de pneumonia, como empiema, que requerem intervenção do procedimento.
|
Conclusões dos autores
|