Nota en base al paper publicado en la revista Plos One:
El laboratorio de Terapia Génica de la Facultad de Ciencias Biomédicas (FCB) y del Hospital Universitario Austral, ha publicado recientemente en la revista Plos One, sus últimos hallazgos acerca de los mecanismos de generación de la fibrosis hepática. En base a la experimentación en ratones y al estudio de muestras de pacientes con diversas patologías hepáticas, se analizó qué rol juega SPARC (proteína secretada, ácida y rica en cisteína) en el proceso que conduce al desarrollo de esta enfermedad.
Se sabe que la fibrosis hepática constituye la antesala de la cirrosis, y que, para esta última, la única solución es el transplante hepático. La acumulación de tejido cicatricial (conocida como fibrosis) en el hígado va disminuyendo progresivamente la funcionalidad del órgano. Una vez establecida la cirrosis pueden generarse distintas complicaciones para el paciente, como el sangrado de varices esofágicas, ictericia, alteraciones de la coagulación, y hasta la aparición de un hepatocarcinoma. La etiología de esta enfermedad es diversa: desde hepatitis crónicas por virus B y C, consumo excesivo de alcohol, enfermedades autoinmunes, metabólicas y farmacológicas.
El laboratorio de Terapia Génica de la Universidad Austral tiene entre sus principales líneas de investigación, el estudio de los mecanismos de la fibrosis hepática y la búsqueda de nuevas estrategias de tratamiento para esta enfermedad.
Con la colaboración del Departamento de Medicina y Nutrición de la Universidad de Carolina del Norte (EE.UU), y del Centro de Investigación Médica Aplicada (CIMA) de la Universidad de Navarra (España), el equipo del laboratorio de Terapia Génica, dirigido por el Dr. Guillermo Mazzolini, propone, en base a sus hallazgos científicos, a SPARC como una potencial “nueva diana” terapéutica para la fibrosis hepática.
De la mano de otros investigadores, como la Dra. Catalina Atorrasagasti, alumna post doctoral de la Facultad de Ciencias Biomédicas (FCB), y del licenciado Estanislao Peixoto, alumno de doctorado de la misma casa de estudios, se han podido confirmar resultados de investigaciones anteriores que manifestaban una relación directa entre la sobre expresión de SPARC y el desarrollo de tejido fibrótico.
El artículo publicado en Plos One, cuyo título es Lack of the Matricellular Protein SPARC Attenuates Liver Fibrogenesis in Mice (La falta de la proteína de matriz celular SPARC, atenúa la fibrogénesis del hígado en ratones), certifica el rol fundamental de SPARC y explica cuáles son los mecanismos a través de los cuáles la inhibición de SPARC puede atenuar el desarrollo de la fibrosis. El método de experimentación consistió en estudiar, en dos modelos experimentales de fibrosis hepática, inducidos por administración de tioacetamida o ligadura del conducto biliar, cuál es el papel desempeñado por SPARC. Empleando ratones de tipo knock out (es decir, modificados genéticamente de modo que no expresaran SPARC), a los cuales se les indujo el estímulo fibrogénico, pudo observarse una atenuación significativa de la magnitud de la fibrosis hepática, en comparación con animales que portaban normalmente el gen que expresa la proteína SPARC, y que mostraron fibrosis avanzada después del daño.
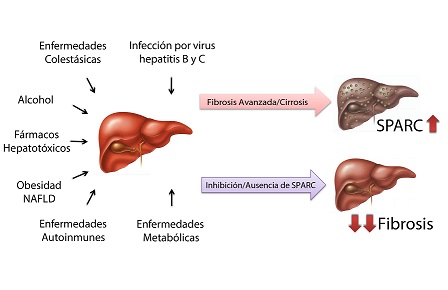
Este equipo de investigación pudo comprobar con anterioridad, como lo demostró en el trabajo publicado en el 2008 en The Journal of Gene Medicine, que la inhibición de SPARC ralentizaba el desarrollo del tejido fibrótico. En aquél entonces se decidió inhibir a SPARC mediante la administración de un adenovirus como herramienta de terapia génica. Pero, el desafío en el trabajo publicado en Plos One fue averiguar qué ocurría con el desarrollo de la fibrosis en el caso de ratones que no sintetizaran a SPARC en ninguna magnitud.
“Esta investigación apuntó a analizar por qué hay un menor desarrollo de la fibrosis en ratones knock out, es decir, ¿cuáles son los mecanismos específicos que permiten una atenuación en el desarrollo de la cirrosis?”, explicó la Dra. Atorrasagasti. Según el Dr. Mazzolini, en base a un análisis de microarreglos de ADN, técnica que permite analizar qué genes se encuentran encendidos y cuáles apagados, los mecanismos que se activan a partir de la inhibición de SPARC en ratones knock out son fundamentalmente de tres tipos: “detoxificación de fármacos, reparación celular y menor inflamación del tejido”.
“Las células responsables de la fibrosis son las llamadas estrelladas o de Ito. Ellas son las que producen colágeno, proteína que luego se transforma en tejido cicatricial. Vimos que ante la ausencia de SPARC, hay menos células de Ito activadas presentes en el tejido hepático”, confirmó el licenciado Peixoto.
“El impacto de la publicación consiste en demostrar que SPARC es una proteína clave en la fibrosis hepática y que las muestras de pacientes con cirrosis de distinta etiología expresan mucho esta proteína, por lo que nos da indicios de que pueda ser una nueva diana terapéutica para el futuro”, sostiene el Dr. Mazzolini.
¿Cuál sería el próximo paso en esta línea de investigación?
G.M: Cuando la cirrosis está establecida, queremos generar una herramienta de terapia génica (vector) que se exprese durante mucho tiempo, incluso durante meses, para que inhiba la expresión de SPARC de modo persistente ¿Es posible revertir la cirrosis? Ese es nuestro siguiente trabajo.