El cáncer colorrectal metastásico con alta inestabilidad de microsatélites (MSI-H) o deficiencia en la reparación de emparejamiento (dMMR) se caracteriza por alteraciones en los mecanismos de reparación del ADN. Estas deficiencias, causadas por mutaciones o silenciamiento epigenético en genes clave, como MLH1, MSH2, MSH6 y PMS2, conducen a la acumulación de errores en secuencias repetitivas del ADN, llamadas microsatélites.
La inestabilidad de microsatélites (MSI) resulta en un fenotipo tumoral altamente mutado e inmunogénico. Los tumores MSI-H/dMMR constituyen aproximadamente el 4-7 % de los casos metastásicos y presentan características clínicas y moleculares únicas, con un comportamiento biológico distinto y una carga mutacional elevada.
Estos tumores tienen un mal pronóstico cuando se tratan con quimioterapia estándar, pero la pérdida funcional de las proteínas de reparación de emparejamiento también actúa como un marcador pronóstico y predictivo relevante. La condición aumenta su sensibilidad a las terapias basadas en inhibidores de puntos de control inmunitario.
En este contexto, la combinación de nivolumab (un inhibidor de PD-1) e ipilimumab (un inhibidor de CTLA-4) ha mostrado una eficacia prometedora, debido a sus mecanismos de acción complementarios, que potencian la respuesta inmunitaria al revertir los mecanismos de evasión tumoral.
El estudio fase 3 CheckMate 8HW evalúa la combinación de nivolumab e ipilimumab, en comparación con la quimioterapia estándar, como tratamiento de primera línea para este subgrupo de pacientes con cáncer colorrectal metastásico MSI-H/dMMR.
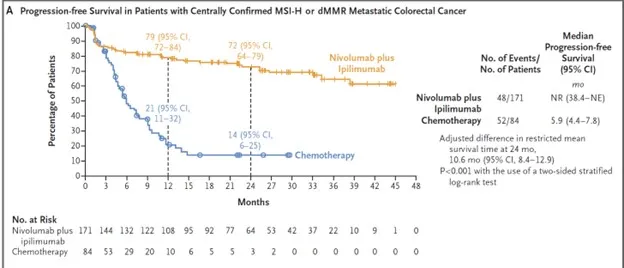
Fue un ensayo multinacional y abierto, donde se asignaron aleatoriamente 303 pacientes no tratados previamente, en una proporción 2:1, a recibir nivolumab más ipilimumab o quimioterapia. Los objetivos primarios fueron la supervivencia libre de progresión (PFS) y la comparación entre los grupos de tratamiento.
En cuanto a los resultados: A los 24 meses, el PFS fue del 72 % en el grupo de nivolumab + ipilimumab contra el 14 % en el grupo de quimioterapia. La media de supervivencia fue 10,6 meses mayor en el grupo que recibió la combinación.
En cuanto a la seguridad: Los eventos adversos graves (grado 3 o 4) fueron menos frecuentes con nivolumab + ipilimumab (23 %) comparado con quimioterapia (48 %). Los efectos secundarios comunes inmunomediados incluyeron prurito, diarrea e hipotiroidismo en el grupo de combinación.
En conclusión: La calidad de vida de los pacientes mejoró significativamente con nivolumab + ipilimumab desde la semana 13, mientras que la quimioterapia mostró un deterioro después de la semana 29. El estudio destaca la importancia de la inmunoterapia en el manejo del cáncer colorrectal MSI-H/dMMR, ofreciendo mejores resultados clínicos.
En estos tipos de tumores, el asesoramiento genético en oncologia (AGO) es de importancia. El AGO desempeña un papel fundamental en el manejo de los pacientes con cáncer colorrectal metastásico MSI-H/dMMR, dado que un porcentaje significativo de estos casos está relacionado con síndromes hereditarios, como el síndrome de Lynch.
El síndrome de Lynch, causado por mutaciones germinales en los genes de reparación de emparejamiento (MLH1, MSH2, MSH6, PMS2 o EPCAM), es la causa hereditaria más común de tumores MSI-H/dMMR. Identificar esta condición tiene implicancias clínicas importantes, ya que permite:
1. Detección temprana: Implementar programas de tamizaje dirigidos, como colonoscopías regulares, para prevenir o detectar en etapas tempranas otros cánceres asociados al síndrome (por ejemplo, de endometrio, ovario, estómago o piel).
2. Orientación familiar: Ofrecer pruebas genéticas predictivas a familiares de primer grado, quienes tienen un 50 % de probabilidad de portar la misma mutación germinal.
3. Planificación del tratamiento: Adaptar estrategias terapéuticas, como el uso preferente de inmunoterapia, dada la alta inmunogenicidad de estos tumores.
La evaluación genética no solo ayuda a confirmar el diagnóstico y guiar el tratamiento, sino también a identificar familiares en riesgo que puedan beneficiarse de estrategias de vigilancia y prevención. Por lo tanto, la integración del AGO no solo mejora los resultados individuales del paciente, sino que también tiene un impacto significativo en la salud pública, al reducir el riesgo de cáncer en familias afectadas.