| Introducción |
La prevalencia global de hipertiroidismo en países con suficiente yodo se estima entre el 0,2% y el 2,5%. La prevalencia del hipertiroidismo manifiesto, definido como niveles bajos de tirorotropina (anteriormente hormona estimulante de la tiroides) con niveles elevados de triyodotironina (T3) y/o tiroxina libre (FT4), es aproximadamente del 0,2% al 1,4%. La prevalencia de hipertiroidismo subclínico, definido como niveles bajos de tirotropina con niveles normales de hormona tiroidea periférica, es aproximadamente del 0,7% al 1,4%.
La tirotoxicosis se refiere a todas las afecciones en las que los niveles de hormona tiroidea están elevados, independientemente del mecanismo subyacente. La tirotoxicosis puede ocurrir debido al hipertiroidismo debido al aumento de la producción de hormona tiroidea, la liberación de hormonas preformadas de la glándula tiroides debido a la inflamación, o el aumento en la disponibilidad extratiroidea de la hormona tiroidea debido a la reposición excesiva de levotiroxina, la ingestión subrepticia de hormona tiroidea o el estruma ovárico, un tipo de tumor dermoide ovárico en el que el tejido tiroideo es el componente predominante del tumor.
El hipertiroidismo no tratado puede causar arritmias cardíacas, insuficiencia cardíaca congestiva, osteoporosis, resultados obstétricos adversos y trastornos metabólicos como aumento del gasto energético en reposo y de la gluconeogénesis.
Esta revisión resume la evidencia actual sobre la fisiopatología, la presentación clínica y el tratamiento del hipertiroidismo, centrándose en el tratamiento de la enfermedad de Graves y la enfermedad nodular tóxica.
Preguntas frecuentes:
| 1. ¿Cómo se debe manejar a los pacientes asintomáticos con hipertiroidismo subclínico? Los resultados anormales de las pruebas de función tiroidea deben confirmarse repitiendo los análisis de sangre en 2 a 3 meses. Si los niveles séricos de tirotropina (anteriormente hormona estimulante de la tiroides) permanecen persistentemente bajos con tiroxina libre normal (FT4) y triyodotironina total (T3), se pueden utilizar pruebas de anticuerpos contra el receptor de tirotropina (TRAb) y posiblemente una gammagrafía tiroidea para determinar la etiología subyacente. El tratamiento con fármacos antitiroideos se recomienda para pacientes mayores de 65 años o para aquellos de 65 años o menos con síntomas, osteoporosis o enfermedad cardíaca cuando el nivel sérico de tirotropina es consistentemente inferior a 0,1 mUI/L. 2. ¿Cuál es el tratamiento de primera línea para la enfermedad de Graves? La mayoría de los pacientes sintomáticos con enfermedad de Graves pueden comenzar a tomar medicamentos antitiroideos para disminuir la síntesis y secreción del exceso de hormona tiroidea. Inicialmente se puede utilizar un bloqueador β para controlar la taquicardia y las palpitaciones en pacientes sintomáticos y se puede suspender una vez que mejoran los niveles de hormona tiroidea. Se pueden considerar opciones de tratamiento definitivas, incluida la tiroidectomía y la ablación con yodo radiactivo, una vez que el hipertiroidismo esté razonablemente controlado. 3. ¿Cómo se debe evaluar a un paciente con bocio nodular en el examen y un nivel de tirotropina sérica persistentemente bajo? Las causas más probables de hipertiroidismo en este contexto incluyen la enfermedad de Graves y el nódulo que funciona de forma autónoma (bocio multinodular tóxico o adenoma tóxico). La ecografía de tiroides puede confirmar la presencia de nódulos y evaluar los riesgos de malignidad de la tiroides. A continuación se debe realizar una gammagrafía tiroidea para determinar la etiología del hipertiroidismo. Esto ayuda a distinguir entre nódulos hiperfuncionantes, que no requieren biopsia, y nódulos hipofuncionantes, que pueden requerir biopsia, según el tamaño y las características ecográficas. |
| Fisiopatología |
La enfermedad de Graves es una enfermedad autoinmune en la que los autoanticuerpos dirigidos contra el receptor de tirotropina tiroidea provocan un aumento de la síntesis y secreción de hormona tiroidea. La enfermedad de Graves es la causa más común de hipertiroidismo en poblaciones repletas de yodo, con una prevalencia del 2% en mujeres y del 0,5% en hombres.
Los nódulos tiroideos con variantes activadoras somáticas en genes que regulan la síntesis hormonal pueden secretar de forma autónoma un exceso de hormona tiroidea, lo que se conoce como enfermedad nodular tóxica. La enfermedad nodular tóxica, la segunda causa más común de hipertiroidismo, es más común en regiones con escasez de yodo, con una incidencia que oscila entre 1,5 y 18 casos por 100.000 personas-año en todo el mundo.
Al principio del embarazo, la gonadotropina coriónica humana (hCG) estimula el receptor tiroideo de tirotropina, provocando un aumento de la síntesis de hormona tiroidea. La autoinmunidad (tiroiditis posparto o esporádica indolora), las infecciones, algunos medicamentos y los traumatismos en la tiroides pueden causar inflamación tiroidea y la liberación de hormonas almacenadas en el torrente sanguíneo, causando tirotoxicosis pero no hipertiroidismo porque no hay aumento en la síntesis de hormona tiroidea.
| Presentación clínica |
Las manifestaciones clínicas de la tirotoxicosis incluyen ansiedad, insomnio, palpitaciones, pérdida de peso por aumento del metabolismo y gasto energético, diarrea o heces blandas, sudoración excesiva, intolerancia al calor y menstruaciones irregulares. Aproximadamente el 2% de las personas mayores con hipertiroidismo presentan hipertiroidismo apático con síntomas mínimos. Pacientes con enfermedad de Graves o nódulos tóxicos pueden informar un aumento del tamaño del cuello o síntomas compresivos debido al agrandamiento de la glándula tiroides, como disfagia, ortopnea o cambios en la voz. El dolor y la sensibilidad tiroideos están presentes en la tiroiditis subaguda, que a menudo va precedida por una infección viral de las vías respiratorias superiores. El hipertiroidismo subclínico suele ser asintomático o causa síntomas similares pero más leves que los del hipertiroidismo manifiesto.
| Evaluación y Diagnóstico |
> Examen físico
Los hallazgos del examen físico pueden variar según los niveles circulantes de hormona tiroidea, la duración del hipertiroidismo y la etiología subyacente. Todas las causas de tirotoxicosis pueden causar taquicardia, hipertensión sistólica, mirada fija, retracción del párpado (cuando el párpado superior permanece elevado al mirar hacia abajo debido a la activación del tono simpático), temblor y debilidad de los músculos proximales. Otros signos son específicos de la etiología de la enfermedad.
La manifestación extratiroidea más común de la enfermedad de Graves es la orbitopatía, que ocurre hasta en el 25% de los pacientes. Esto se presenta como eritema conjuntival, edema periorbitario, retracción palpebral y proptosis. Otras manifestaciones extratiroideas de la enfermedad de Graves incluyen mixedema pretibial (pápulas induradas de color rosa o púrpura, a veces acompañadas de linfedema y elefantiasis en la parte anterior de la pierna), que ocurre en aproximadamente el 1,5% de los pacientes, y acropaquia (hinchazón de los dedos y uñas en palillo de tambor), que ocurre en aproximadamente el 0,3% de los pacientes.
> Pruebas de laboratorio
Un nivel bajo de tirotropina sérica es la mejor prueba para detectar la disfunción tiroidea y tiene la mayor sensibilidad (92% -95%) y especificidad (89% -85%). Los valores se pueden utilizar para evaluar el grado de hipertiroidismo. Los niveles también pueden ayudar a establecer la causa y la gravedad de la tirotoxicosis. La proporción T3 total:T4 suele ser superior a 20:1 en la enfermedad de Graves o nódulos tóxicos, pero inferior a 20:1 en la tiroiditis.
Una vez confirmada la tirotoxicosis, se debe determinar la etiología (Figura 1). La presencia de anticuerpos anti-receptores de tirotropina (TRAbs) es patognomónico de la enfermedad de Graves. Las directrices actuales recomiendan medir los niveles de TRAb como paso inicial para diferenciar la enfermedad de Graves de otras causas de tirotoxicosis.

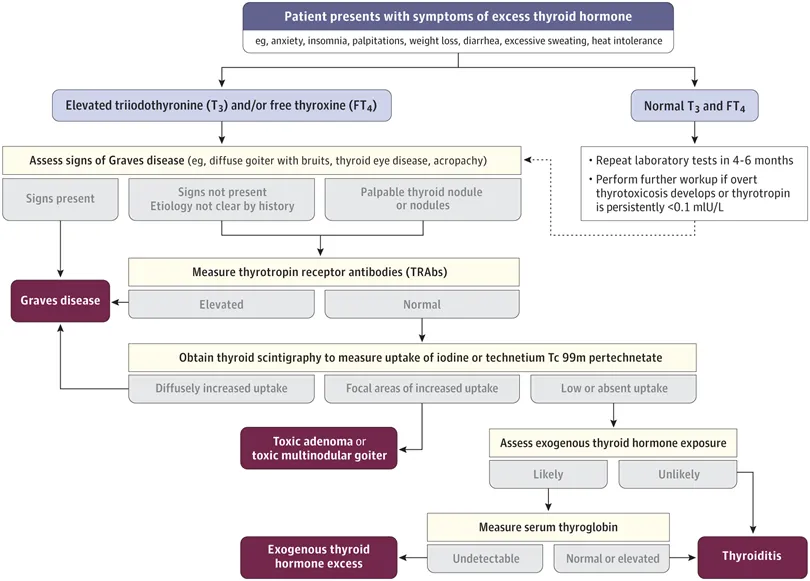
Figura 1. Algoritmo en Tirotoxicosis
> Estudios de imagen
Se recomienda la gammagrafía tiroidea con yodo radiactivo o pertecnetato de tecnecio 99m (Tc 99m) si hay nódulos tiroideos palpables o si la etiología de la tirotoxicosis no está clara después de la prueba de TRAb. La captación de yodo radiactivo aumenta de forma difusa en la enfermedad de Graves y de forma focal o heterogénea en los adenomas o nódulos tóxicos. La absorción de yodo radiactivo es baja o nula en la tiroiditis, la exposición elevada al yodo o las fuentes extratiroideas de la hormona tiroidea.
| Tratamiento |
Las opciones de tratamiento deben basarse en la etiología subyacente. En pacientes con enfermedad de Graves, el tratamiento debe centrarse en controlar el hipertiroidismo con una eventual remisión anticipada, mientras que las causas de hipertiroidismo debido a enfermedad nodular tóxica requieren tratamiento indefinido si se utilizan fármacos antitiroideos porque este no remite (Figura 2)
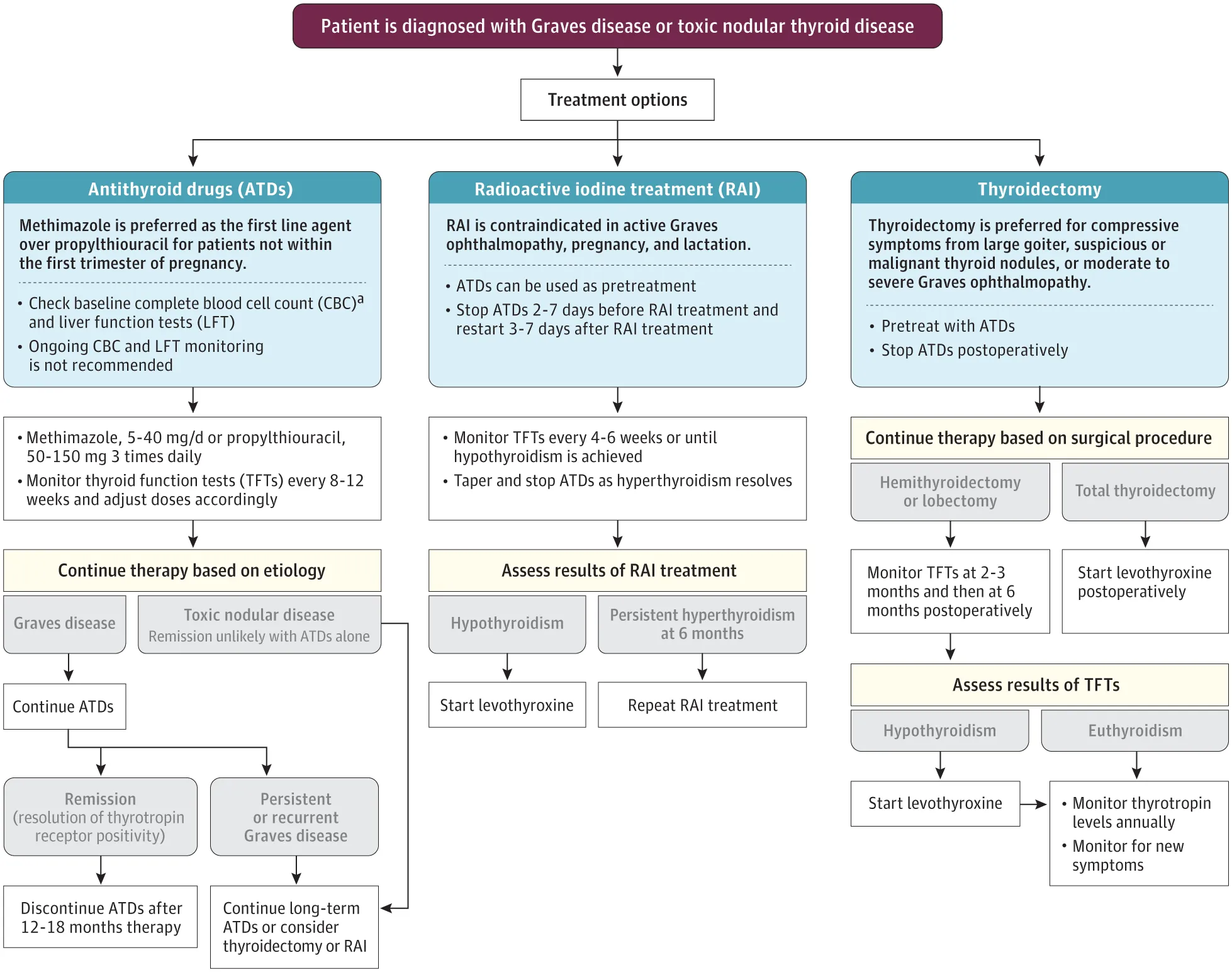

Figura 2. Tratamiento del Hipertiroidismo
Los pacientes sintomáticos con todas las formas de tirotoxicosis pueden beneficiarse del inicio de betabloqueantes, que disminuyen la frecuencia cardíaca y mejoran los síntomas hiperadrenérgicos pero está relativamente contraindicado en pacientes con enfermedad broncoespástica. El bloqueo β suele ser el único tratamiento necesario para la tirotoxicosis debida a tiroiditis porque este trastorno es autolimitado y no hay indicación de tratamiento con fármacos antitiroideos en ausencia de un aumento de la síntesis de hormona tiroidea.
La mayoría de los pacientes con hipertiroidismo manifiesto por nódulos tiroideos autónomos o enfermedad de Graves requerirán tratamiento con fármacos antitiroideos, ablación con yodo radiactivo o cirugía.
> Medicamentos antitiroideos
Las tionamidas (metimazol; carbimazol, que se metaboliza a metimazol; y propiltiouracilo) disminuyen la síntesis y secreción de hormona tiroidea y pueden restablecer el eutiroidismo en pacientes con hipertiroidismo. El metimazol es el agente de primera línea para personas que no se encuentran en el primer trimestre del embarazo.
Las pruebas de función tiroidea deben controlarse cada 4 a 8 semanas después del inicio del tratamiento y el metimazol a menudo puede ajustarse hasta una dosis de mantenimiento de 5 a 10 mg/día a medida que mejora el hipertiroidismo en la enfermedad de Graves. Para los pacientes con nódulos tiroideos autónomos, las dosis requeridas de metimazol suelen ser de 10 mg/día o menos, y las pruebas de función tiroidea deben vigilarse cada tres meses al menos al principio.
Para los pacientes con enfermedad de Graves, el tratamiento con fármacos antitiroideos se puede suspender después de 12 a 18 meses si los niveles séricos de tirotropina se han normalizado y el paciente ya no da positivo para TRAb.
Se debe asesorar cuidadosamente a los pacientes sobre los posibles efectos adversos de los fármacos antitiroideos antes de iniciar el tratamiento. En general, se informan efectos adversos en aproximadamente el 13% de los pacientes. El efecto adverso más frecuente es el prurito y/o erupción, que ocurre en el 6% de los que toman metimazol y en el 3% de los que toman propiltiouracilo. Por lo general, ambos efectos adversos se pueden controlar con antihistamínicos.
> Tratamiento con yodo radioactivo
El tratamiento con yodo radiactivo cura el hipertiroidismo en más del 90% de los pacientes con enfermedad de Graves o nódulos tiroideos autónomos. Se recomienda el bloqueo β y el metimazol previo al tratamiento en pacientes de edad avanzada y en aquellos con riesgo particularmente alto de sufrir eventos cardiovasculares en caso de empeoramiento transitorio del hipertiroidismo después del tratamiento con yodo radiactivo. Si se usa, el metimazol debe suspenderse de 2 a 7 días antes del tratamiento y puede reiniciarse de 3 a 7 días después.
El objetivo del tratamiento en la enfermedad de Graves es provocar hipotiroidismo en el paciente, mientras que en el bocio nodular tóxico el objetivo es aliviar el hipertiroidismo. El yodo radiactivo puede causar o exacerbar enfermedades oculares entre pacientes con enfermedad de Graves, particularmente en aquellos que fuman cigarrillos o con títulos de TRAb muy altos. Para prevenir esto, se debe utilizar un pretratamiento con prednisona de 0,3 mg/kg a 0,5 mg/kg por día, disminuyendo gradualmente durante 3 meses, en personas que fuman cigarrillos, en aquellas con niveles altos de TRAb o en aquellas con enfermedad ocular tiroidea preexistente.
> Procedimientos quirúrgicos
La tiroidectomía está indicada para pacientes con hipertiroidismo que tienen síntomas de compresión local debido a un bocio grande, nódulos tiroideos sospechosos o malignos u oftalmopatía de moderada a grave por enfermedad de Graves. La tiroidectomía debe ser el tratamiento de primera línea si se confirma o sospecha una neoplasia maligna tiroidea concurrente.
Entre los pacientes con enfermedad de Graves, la tiroidectomía total se asocia con un riesgo menor de hipertiroidismo recurrente que la tiroidectomía subtotal y es la operación preferida. En personas con adenoma tóxico, se puede preferir la lobectomía tiroidea a la del yodo radiactivo cuando se prefiere una resolución rápida, por motivos estéticos o si hay síntomas de compresión local debido a una glándula tiroides grande. La tiroidectomía total cura rápidamente el hipertiroidismo causado por la enfermedad de Graves o el bocio multinodular tóxico, pero resulta en una necesidad de por vida de terapia de reemplazo de hormona tiroidea.
| Hipertiroidismo subclínico |
El hipertiroidismo subclínico puede resolverse espontáneamente y progresar a hipertiroidismo manifiesto en aproximadamente el 8% de los pacientes al año y el 26% al quinto año. La progresión a hipertiroidismo manifiesto es más común en personas con un nivel sérico de tirotropina indetectable al inicio del estudio y en aquellos con bocio multinodular tóxico.
El Grupo de Trabajo de Servicios Preventivos de EE. UU. Actualmente recomienda no realizar pruebas ni tratar el hipertiroidismo subclínico. Sin embargo, otras guías estadounidenses y europeas recomiendan el tratamiento del hipertiroidismo subclínico cuando se identifica en pacientes mayores de 65 años (o menores de 65 años con síntomas, osteoporosis o enfermedad cardíaca) cuando el nivel de tirotropina sérica es consistentemente inferior a 0,1 mUI/L.
| Embarazo y lactancia |
La tirotoxicosis gestacional transitoria, en la que la producción de hormona tiroidea aumenta debido a la estimulación tiroidea por niveles elevados de hCG, afecta aproximadamente del 2 al 11% de los embarazos y se asocia con hiperemesis gravídica. Esta afección no requiere tratamiento con fármacos antitiroideos y no se asocia con resultados obstétricos adversos. Puede controlarse simplemente con pruebas seriadas de la función tiroidea y se resuelve espontáneamente a medida que disminuyen los niveles maternos de hCG. Todas las demás formas de hipertiroidismo manifiesto en el embarazo requieren tratamiento para reducir los riesgos de resultados que incluyen preeclampsia, bajo peso al nacer, aborto espontáneo y parto prematuro.
| Tormenta tiroidea |
La tormenta tiroidea consiste en un hipertiroidismo severo no controlado y se caracteriza por una falla multiorgánica y una tasa de mortalidad del 3,6% al 17%. Los síntomas de presentación pueden incluir fiebre, taquicardia, insuficiencia cardíaca, fibrilación auricular y diversas anomalías del sistema nervioso central. La tormenta tiroidea puede ser precipitada por la cirugía, el uso de amiodarona o la interrupción de los fármacos antitiroideos.
| Conclusión |
El hipertiroidismo afecta al 2,5% de los adultos en todo el mundo y se asocia con osteoporosis, enfermedades cardíacas y aumento de la mortalidad. Los tratamientos de primera línea son los fármacos antitiroideos, la cirugía de tiroides y el tratamiento con yodo radiactivo. Las opciones de tratamiento deben ser individualizadas y centradas en el paciente.